Esperoct®
Information destinée aux patients en Suisse
Qu’est-ce que l’Esperoct et quand doit-il être utilisé ?
Esperoct contient le principe actif turoctocog alfa pégol, une préparation de facteur de coagulation VIII recombinant à longue durée d’action. Le facteur VIII est une protéine présente dans le sang qui favorise la coagulation sanguine.
Esperoct est utilisé sur prescription du médecin pour le traitement et la prévention des hémorragies chez les patients atteints d’hémophilie A (déficit congénital en facteur VIII) et peut être utilisé dans tous les groupes d’âge.
Chez les patients atteints d’hémophilie A, le facteur VIII est absent ou ne fonctionne pas correctement. Esperoct remplace ce facteur VIII manquant ou défectueux et soutient la formation de caillots sanguins au site de l’hémorragie.
Esperoct ne contient pas de facteur von Willebrand et ne doit donc pas être utilisé pour le traitement du syndrome de von Willebrand-Jürgens.
Quand Esperoct ne doit-il pas être utilisé ?
Esperoct ne doit pas être utilisé,
– si vous êtes allergique au principe actif ou à l’un des autres composants de ce médicament (voir sous «Que contient Esperoct ?»);
– si vous êtes allergique aux protéines de hamster.
N’utilisez pas Esperoct si une de ces situations vous concerne. Si vous avez des doutes, veuillez consulter votre médecin avant d’utiliser le médicament.
Quelles sont les précautions à observer lors de l’utilisation d’Esperoct ?
Utilisation antérieure d’une préparation de facteur VIII
Informez votre médecin si vous avez déjà été traité(e) avec des médicaments à base de facteur VIII, surtout si vous avez développé des anticorps, car il peut y avoir un risque accru que cela se reproduise.
Réactions allergiques
Il existe la possibilité de développer une réaction allergique sévère et soudaine (p.ex. une réaction anaphylactique) à Esperoct.
Si vous avez des signes précurseurs d’une réaction allergique, cessez immédiatement l’injection et contactez votre médecin. Les premiers signes d’une réaction allergique sont une éruption cutanée, de l’urticaire, des papules, des démangeaisons sur de grandes surfaces de la peau, une rougeur et/ou un gonflement des lèvres, du visage et de la langue, des difficultés à déglutir ou à respirer, un essoufflement, une respiration sifflante, une sensation d’oppression dans le thorax, une peau pâle et froide, un rythme cardiaque rapide ou des étourdissements.
Formation d’inhibiteurs (anticorps) du facteur VIII
Les inhibiteurs (anticorps) peuvent survenir pendant le traitement avec tous les médicaments contenant le facteur VIII.
– Ces inhibiteurs empêchent une efficacité adéquate du médicament, en particulier à des concentrations élevées.
– Vous devez faire l’objet d’une surveillance étroite concernant le développement de ces inhibiteurs.
– Si vos saignements ne peuvent pas être contrôlés avec Esperoct, informez-en immédiatement votre médecin.
– N’augmentez pas la dose totale d’Esperoct sans en avoir parlé à votre médecin.
Problèmes liés aux cathéters
Si vous avez un cathéter par lequel le médicament peut être injecté dans votre sang (cathéter veineux central), des infections ou des caillots sanguins peuvent se produire au site du cathéter.
Trouble cardiaque
Adressez-vous à votre médecin ou à votre pharmacien si vous souffrez d’un trouble cardiaque ou si vous présentez un risque connu de trouble cardiaque.
Utilisation d’Esperoct avec d’autres médicaments
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie,
– si vous êtes allergique
– ou si vous utilisez déjà d’autres médicaments en usage interne ou externe (même en automédication!).
Aptitude à la conduite et capacité à utiliser des machines
Esperoct n’affecte pas l’aptitude à conduire et la capacité à utiliser des machines.
Esperoct contient du sodium.
Ce médicament contient, après reconstitution, 30,5 mg de sodium par flacon perforable. Consultez votre médecin si vous devez veiller à une alimentation pauvre en sodium.
Activité réduite du facteur VIII chez les patients précédemment traités
Au début de votre traitement, il est possible que l’activité du facteur VIII soit réduite. Veuillez informer votre médecin si vous pensez que votre médicament est moins efficace que prévu.
Réaction du système immunitaire chez les patients non précédemment traités
Au début du traitement, il est possible que des réactions transitoires du système immunitaire apparaissent, pouvant se traduire par une moindre efficacité de votre médicament.
Esperoct peut-il être utilisé pendant la grossesse ou l’allaitement ?
Si vous êtes enceinte ou si vous allaitez, si vous suspectez une grossesse ou si vous prévoyez de tomber enceinte, veuillez consulter votre médecin avant d’utiliser ce médicament.
Comment utiliser Esperoct ?
Le traitement par Esperoct est instauré par un médecin expérimenté dans le traitement de patients atteints d’hémophilie A. Utilisez ce médicament en vous conformant strictement aux prescriptions de votre médecin. Veuillez demander conseil à votre médecin si vous avez des doutes sur l’utilisation d’Esperoct.
Administration d’Esperoct
Esperoct est administré par injection dans une veine (par voie intraveineuse). Pour de plus amples informations, voir sous «Remarques concernant l’administration d’Esperoct».
Posologie
Votre médecin calculera la dose nécessaire pour vous. Celle-ci dépend de votre poids corporel ainsi que de l’utilisation qui en est faite pour prévenir ou traiter un saignement.
Prévention des hémorragies
– Adultes et adolescents (à partir de 12 ans): la dose initiale recommandée est de 50 UI d’Esperoct par kg de poids corporel tous les 4 jours. Celle-ci peut être ajustée tous les 3 à 4 jours.
Chez certains patients, la dose peut être augmentée à 75 UI par kg de poids corporel tous les 7 jours. Celle-ci dépend de la façon dont le patient réagit au médicament et de la recommandation du médecin traitant.
– Enfants (de moins de 12 ans): la dose initiale recommandée est de 50 à 75 UI d’Esperoct par kg de poids corporel. Le médicament est administré deux fois par semaine.
Traitement des hémorragies
La dose d’Esperoct est calculée en fonction de votre poids corporel et des taux de facteur VIII à atteindre. Le taux de facteur VIII cible dépend du site de l’hémorragie et de son intensité. Si vous avez l’impression que l’effet d’Esperoct n’est pas suffisant, contactez votre médecin.
Utilisation chez les enfants et les adolescents
Esperoct peut être utilisé chez les enfants de toutes les tranches d’âge. Les enfants (de moins de 12 ans) peuvent avoir besoin de doses plus élevées ou d’injections plus fréquentes. Les enfants (de plus de 12 ans) et les adolescents peuvent utiliser la même dose que les adultes.
Si vous administrez plus d’Esperoct que vous ne le devriez
Si vous avez administré plus d’Esperoct que vous ne le devriez, veuillez en informer votre médecin.
Si vous devez utiliser beaucoup plus d’Esperoct pour arrêter les hémorragies, veuillez en informer immédiatement votre médecin. Vous trouverez de plus amples informations dans la section «Formation d’inhibiteurs (anticorps) du facteur VIII».
Si vous avez oublié d’utiliser Esperoct
Si vous oubliez une dose, injectez-la dès que vous vous en rendez compte. N’injectez pas une double dose pour compenser la dose oubliée. Faites la prochaine injection comme prévu et continuez selon les directives de votre médecin. En cas de doute, contactez votre médecin.
Si vous arrêtez d’utiliser Esperoct
N’interrompez pas le traitement avec Esperoct sans consulter votre médecin.
Si vous arrêtez d’utiliser Esperoct, il se pourrait que vous ne soyez plus protégé(e) contre les hémorragies, ou une hémorragie en cours pourrait ne plus s’arrêter. Si vous avez des questions supplémentaires sur l’utilisation de ce médicament, veuillez consulter votre médecin.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Esperoct peut-il provoquer ?
Comme tous les médicaments, ce médicament peut provoquer des effets secondaires, même si ces derniers n’apparaissent pas chez tous les patients.
Réactions allergiques (hypersensibilité)
En cas de réactions allergiques sévères et soudaines (réactions anaphylactiques), l’injection doit être interrompue immédiatement. Consultez immédiatement votre médecin si vous constatez l’un des symptômes suivants d’une réaction allergique:
– une difficulté à déglutir ou à respirer
– un essoufflement ou une respiration sifflante
– une sensation d’étau dans la cage thoracique
– une rougeur et/ou un gonflement des lèvres, de la langue, du visage ou des mains
– une éruption cutanée, de l’urticaire, des papules ou des démangeaisons
– peau pâle et froide, rythme cardiaque rapide ou étourdissements (hypotension)
Formation d’inhibiteurs (anticorps) du facteur VIII
Chez les enfants qui n’ont encore jamais été traités par des médicaments contenant le facteur VIII, il est très fréquent (plus de 1 patient sur 10) de développer des anticorps anti-facteur VIII (voir «Quelles sont les précautions à observer lors de l’utilisation d’Esperoct ?»).
Si vous avez déjà été traité(e) avec le facteur VIII pendant plus de 150 jours, des inhibiteurs (anticorps) peuvent survenir (chez moins de 1 patient sur 100). Si cela se produit, votre médicament pourrait ne plus fonctionner correctement et vous pourriez avoir des hémorragies prolongées. Si cela se produit, contactez immédiatement avec votre médecin. Voir «Formation d’inhibiteurs (anticorps) du facteur VIII» sous «Quelles sont les précautions à observer lors de l’utilisation d’Esperoct ?».
Les effets indésirables suivants ont été observés avec Esperoct
Très fréquent (concerne plus de 1 personne sur 10)
– Inhibition du facteur VIII chez des patients non précédemment traités
Fréquent (concerne 1 à 10 personnes sur 100)
– Réactions cutanées (rougeurs et démangeaisons) dans la zone autour du site où vous avez injecté le médicament
– Démangeaisons (prurit)
– Rougeur de la peau (érythème)
– Éruption cutanée
– Réactions allergiques (hypersensibilité) chez des patients n’ayant jamais été traités avec le facteur VIII auparavant. Ces réactions peuvent être sévères et mettre la vie en danger. Pour plus d’informations, voir «Réactions allergiques (hypersensibilité)» ci-dessus.
Occasionnel (concerne 1 à 10 personnes sur 1000)
– Réactions allergiques (hypersensibilité) chez les patients qui ont déjà été traités avec le facteur VIII. Ces réactions peuvent être sévères et mettre la vie en danger. Pour plus d’informations, voir «Réactions allergiques (hypersensibilité)» ci-dessus.
– Développement d’inhibiteurs du facteur VIII (anticorps) chez les patients ayant déjà été traités avec le facteur VIII
Fréquence inconnue (ne peut être estimée sur la base des données disponibles)
Activité réduite du facteur VIII en l’absence d’inhibiteurs du facteur VIII.
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Stabilité
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient. La date imprimée se rapporte au dernier jour du mois en question et est indiquée sur l’emballage en carton, sur l’étiquette du flacon perforable et de la seringue.
Avant la reconstitution (avant le mélange de la poudre avec le solvant):
À conserver au réfrigérateur (entre 2°C et 8°C).
Esperoct peut être conservé avant la date de péremption
– à température ambiante (jusqu’à 30°C) pendant une période de 12 mois au maximum ou
– au-dessus de la température ambiante (>30°C jusqu’à 40°C) pendant trois mois au maximum.
Quand vous commencez à conserver Esperoct en dehors du réfrigérateur, veuillez noter la date du début de la conservation et la température de conservation d’Esperoct® à l’endroit prévu à cet effet sur le carton d’emballage.
Une fois que le produit a été conservé hors du réfrigérateur, il ne doit plus y être replacé dans le but d’y être conservé.
Délai d’utilisation après ouverture
Après la reconstitution (après le mélange de la poudre avec le solvant):
Une fois que vous avez reconstitué Esperoct, vous devez l’utiliser immédiatement. Si vous ne pouvez pas utiliser la solution reconstituée immédiatement, vous devez l’utiliser dans les:
– 24 heures si elle a été conservée au réfrigérateur (entre 2 et 8°C) ou
– 4 heures si elle a été conservée à ≤30°C ou
– 2 heures entreposée entre >30°C et 40°C pour les produits qui, avant reconstitution n’ont pas été conservés plus de 3 mois au-dessus la température ambiante (>30°C jusqu’à 40°C).
Conservez le produit reconstitué dans le flacon perforable.
La poudre dans le flacon perforable est blanche voire grise blanche. N’utilisez pas la poudre si la couleur a changé.
La solution reconstituée doit être claire et incolore. N’utilisez pas la solution reconstituée si vous remarquez qu’elle est trouble ou qu’elle contient des particules visibles.
Remarques concernant le stockage
Conserver au réfrigérateur (2-8°C). Ne pas congeler. Protéger le produit de la lumière dans l’emballage d’origine.
Conserver hors de portée des enfants.
Remarques complémentaires
Ne jetez jamais les médicaments dans les eaux usées ou les déchets ménagers. Demandez à votre pharmacien comment éliminer les médicaments que vous n’utilisez plus. Vous contribuez ainsi à préserver l’environnement.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Esperoct ?
Substance active: turoctocog alfa pégol (facteur VIII de coagulation humain pégylé (ADNr)). Chaque flacon d’Esperoct contient nominalement 500, 1000, 1500, 2000 ou 3000 UI de turoctocog alfa pégol.
Excipients: L-histidine, saccharose, polysorbate 80, chlorure de sodium, L-méthionine, chlorure de calcium dihydraté, hydroxyde de sodium et acide chlorhydrique.
Solvant: solution de chlorure de sodium 9 mg/ml (0,9%) pour injection et eau pour solutions injectables.
Après la préparation avec la solution jointe à l’emballage (solution de chlorure de sodium 9 mg/ml [= 0,9%] pour injection), la solution à injecter prête à l’emploi contient 125, 250, 375, 500 ou 750 UI de turoctocog alfa pégol par ml (selon la dose de turoctocog alfa pégol, soit 500, 1000, 1500, 2000 ou 3000 UI).
Numéro d’autorisation
67156 (Swissmedic)
Où obtenez-vous Esperoct ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, uniquement sur ordonnance médicale.
Esperoct est disponible en emballages de 500, 1000, 1500, 2000 ou 3000 UI.
Chaque emballage d’Esperoct contient:
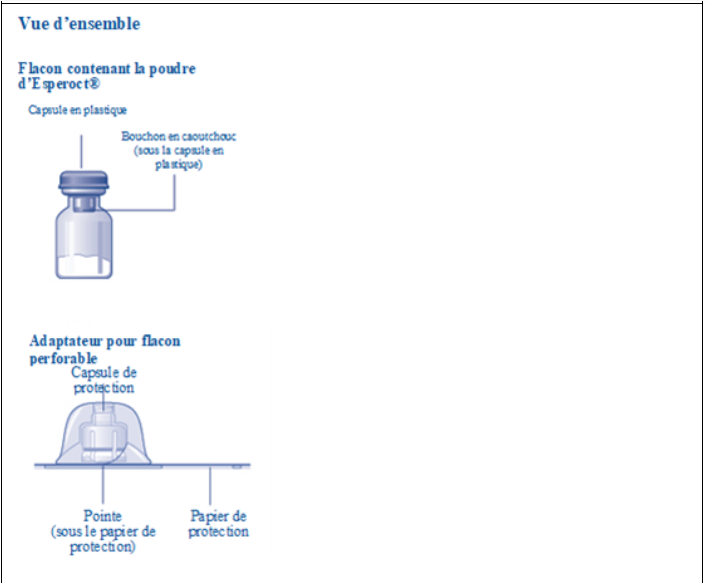
– 1 flacon perforable avec une poudre blanche voire grise blanche
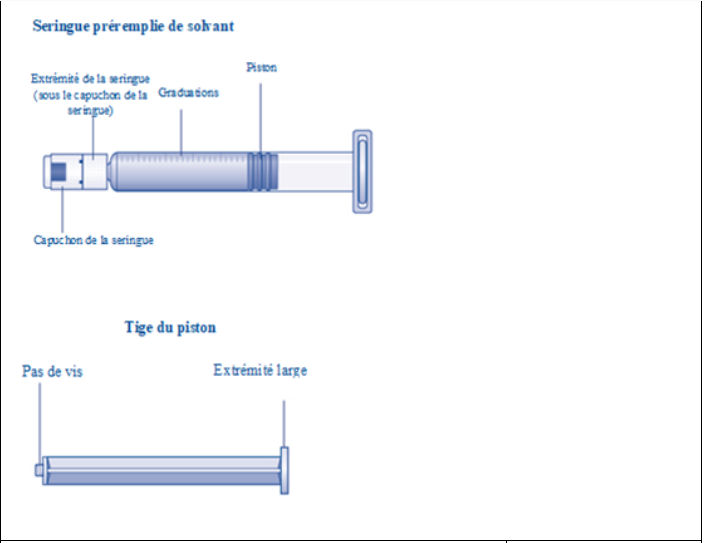
– 1 seringue préremplie de 4 ml de solvant limpide et incolore
– 1 tige de piston
– 1 adaptateur pour flacon perforable
Titulaire de l’autorisation
Novo Nordisk Pharma AG, Kloten
Domicile: Zürich
Fabricant
Novo Nordisk A/S, DK-2880 Bagsværd
Cette notice d’emballage a été vérifiée pour la dernière fois en avril 2023 par l’autorité de contrôle des médicaments (Swissmedic).
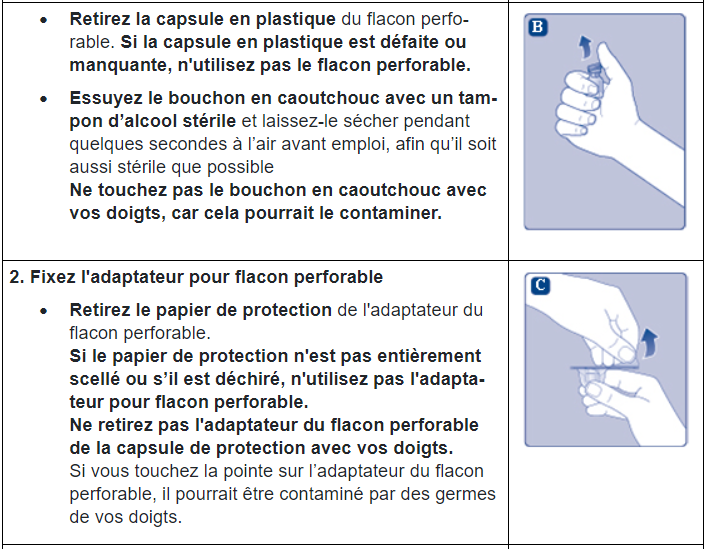
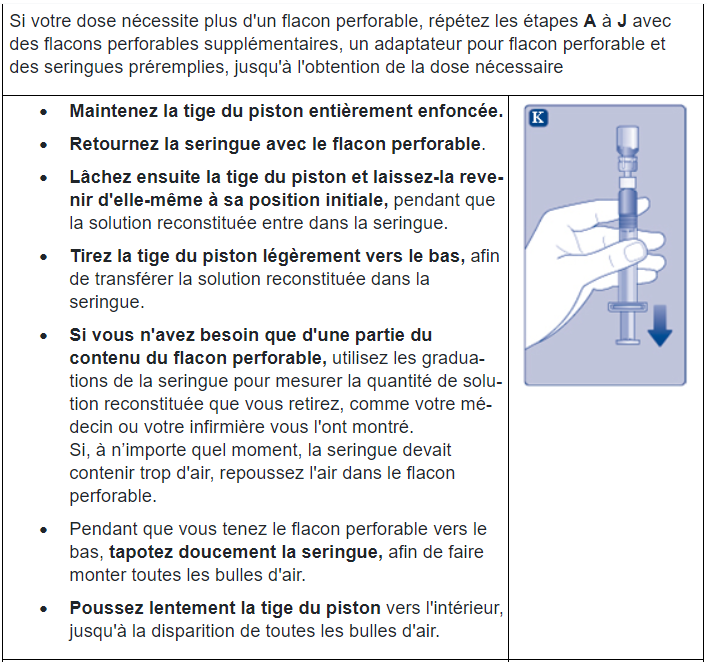
Instructions d’utilisation d’Esperoct








Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 06.07.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère publication de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


