Fulphila® solution injectable en seringue préremplie disposant d’un système de protection de l’aiguille
Information destinée aux patients en Suisse
Qu’est-ce que Fulphila et quand doit-il être utilisé ?
Selon prescription du médecin.
Fulphila contient comme principe actif le pegfilgrastim. Le pegfilgrastim contient une protéine produite par biotechnologie à partir d’une bactérie appelée E. coli. Le pegfilgrastim, appartient au groupe des protéines appelées cytokines et est très proche d’une protéine naturelle (le facteur de croissance granulocytaire) produite par l’organisme.
Fulphila est utilisé pour réduire la durée des neutropénies (faible nombre de globules blancs dans le sang) et l’apparition d’une neutropénie fébrile (faible nombre de globules blancs associé à de la fièvre) qui peuvent être dues à l’utilisation d’une chimiothérapie cytotoxique (médicaments qui détruisent des cellules en croissance rapide). Les globules blancs sont importants, car ils aident votre organisme à combattre les infections. Ces globules blancs sont très sensibles aux effets de la chimiothérapie qui peut en diminuer le nombre dans l’organisme. Si le nombre de globules blancs diminue jusqu’à un taux faible, l’organisme peut ne plus avoir suffisamment de ces cellules pour combattre les bactéries et le risque d’infection peut augmenter.
Votre médecin vous a prescrit Fulphila pour stimuler votre moelle osseuse (partie de l’os qui produit les globules sanguins) afin qu’elle fabrique plus de globules blancs qui aident l’organisme à lutter contre les infections.
Fulphila doit être utilisé uniquement sur prescription du médecin.
De quoi faut-il tenir compte en dehors du traitement ?
Fulphila est destiné à l’utilisation par des adultes âgés de 18 ans minimum et pesant au moins 45 kg.
Quand Fulphila ne doit-il pas être utilisé ?
Fulphila ne doit pas être utilisé si vous êtes hypersensible (allergique) au principe actif pegfilgrastim, au filgrastim, aux protéines dérivées d’E. coli ou à l’un des autres composants de Fulphila.
Quelles sont les précautions à observer lors de l’utilisation de Fulphila ?
Veuillez informer votre médecin ou votre pharmacien si:
– vous toussez, si vous avez de la fièvre et présentez des difficultés à respirer;
– vous avez des signes soudains d’allergie tels qu’éruption cutanée, démangeaisons ou urticaire, gonflement du visage, des lèvres, de la langue ou d’autres parties du corps, essoufflement, respiration sifflante ou difficulté à respirer, ceux-ci pourraient être les signes d’une réaction allergique sévère;
– vous avez des symptômes d’ inflammation de l’aorte (le grand vaisseau sanguin qui achemine le sang du cœur dans le corps). Ceci a été signalé à une fréquence rare chez les patients atteints d’un cancer et les donneurs sains. Les symptômes peuvent comprendre: fièvre, douleurs abdominales, malaise, maux de dos ou augmentation des marqueurs inflammatoires. Si vous ressentez ces symptômes, parlez-en à votre médecin;
– vous avez connaissance d’une modification de votre numération des cellules sanguines (par exemple une augmentation du nombre de globules blancs ou une anémie) ou une diminution du nombre de plaquettes sanguines, ce qui réduit la capacité du sang à coaguler (thrombopénie). Votre médecin peut vouloir vous surveiller plus étroitement;
– vous êtes atteint(e) d’anémie falciforme;
– vous êtes atteint(e) d’un cancer du sein ou du poumon, Fulphila associé à la chimiothérapie et/ou à la radiothérapie peut augmenter le risque pour vous de développer une affection précancéreuse appelée syndrome myélodysplasique (SMD) ou un cancer du sang appelé leucémie myéloïde aiguë (LMA). Les symptômes peuvent inclure la fatigue, la fièvre et l’apparition facile d’ecchymoses ou de saignements;
– vous souffrez d’une douleur abdominale haute à gauche ou d’une douleur au niveau de l’épaule;
– vous souffrez d’une autre maladie;
– vous prenez ou utilisez déjà d’autres médicaments en usage externe (même en auto-médication)!
Votre médecin effectuera des analyses régulières de votre sang et de vos urines, étant donné que Fulphila peut endommager les minuscules filtres de vos reins (glomérulonéphrite).
Des réactions cutanées sévères (syndrome de Stevens-Johnson) ont été rapportées lors de l’utilisation de Fulphila. Arrêtez le traitement par Fulphila si vous remarquez l’un des symptômes décrits ci-dessous:
– Syndrome de Stevens-Johnson, qui peut apparaître sous la forme de taches rougeâtres ressemblant à une cible ou de taches circulaires présentant souvent des cloques en leur centre et situées sur le tronc, d’une desquamation de la peau et d’ulcérations au niveau de la bouche, de la gorge, du nez, des parties génitales et des yeux, et qui peut être précédé de fièvre ou de symptômes s’apparentant à ceux de la grippe. Si l’un de ces symptômes apparaît, il convient de cesser d’utiliser Fulphila et de consulter immédiatement un médecin.
Perte de réponse à Fulphila
Si vous remarquez une perte ou une diminution de l’efficacité du traitement par Fulphila, votre médecin en recherchera les raisons et contrôlera si vous avez développé des anticorps qui diminuent l’effet de Fulphila.
Fulphila contient du sorbitol et de l’acétate de sodium.
Le sorbitol est une source de fructose. Si vous présentez une intolérance héréditaire au fructose (IHF), une maladie génétique rare, vous ne devez pas recevoir ce médicament. Les patients atteints d’IHF ne peuvent pas décomposer le fructose, et ne doivent pas recevoir ce médicament en raison de risque d’effets indésirables graves.
Vous devez en informer votre médecin avant de recevoir ce médicament si vous présentez une IHF.Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose de 6 mg, c’est-à-dire qu’il peut être considéré comme «sans sodium».
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie
– vous êtes allergique
– vous prenez déjà d’autres médicaments (ou utilisez déjà d’autres médicaments en usage externe) (même en automédication!).
Fulphila peut-il être utilisé pendant la grossesse ou l’allaitement ?
Demandez conseil à votre médecin ou à votre pharmacien avant de prendre tout médicament. Fulphila n’a pas été étudié chez la femme enceinte. Il est important de signaler à votre médecin si vous:
– êtes enceinte;
– penser être enceinte; ou
– envisagez d’être enceinte.
Vous devez arrêter l’allaitement si vous utilisez Fulphila
Comment utiliser Fulphila ?
Utilisez toujours Fulphila en suivant exactement les instructions de votre médecin. En cas d’incertitude, consultez votre médecin ou votre pharmacien.
La dose habituelle est 6 mg (1 seringue préremplie contenant 0,6 ml de solution injectable) injectée par voie sous-cutanée (injection sous la peau) environ 24 heures après votre dernière dose de chimiothérapie à la fin de chacun des cycles (cures de traitement). Fulphila ne doit pas être administré durant l’intervalle compris entre les 14 jours précédant et les 24 heures suivant une chimiothérapie cytotoxique.
Votre médecin a décidé qu’il était préférable que vous pratiquiez vous-même les injections de Fulphila. Votre médecin ou le personnel soignant vous montreront comment procéder. N’essayez pas de vous faire une injection avant d’avoir reçu de formation.
Veuillez lire les instructions concernant l’auto-injection de Fulphila à la fin de cette notice d’emballage.
Si vous avez injecté plus de Fulphila que vous n’auriez dû
Si vous avez administré plus de Fulphila que vous ne deviez, contactez votre médecin, le personnel soignant ou votre pharmacien.
Si vous avez oublié de vous injecter Fulphila
Si vous avez oublié une injection de Fulphila, contactez votre médecin pour fixer avec lui la date de la prochaine injection.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Fulphila peut-il provoquer ?
Comme tous les médicaments, Fulphila peut provoquer des effets indésirables, mais ils ne surviennent pas systématiquement chez tout le monde.
Veuillez contacter immédiatement votre médecin si vous ressentez un ou plusieurs des effets indésirables ci-dessous:
– boursoufflure ou gonflement, qui peuvent être associés à une émission d’urine plus rare, des difficultés respiratoires, un gonflement dans la cavité abdominale, une pesanteur d’estomac, et une sensation de fatigue générale. Ces symptômes apparaissent généralement de façon très rapide.
Ceux-ci peuvent être les symptômes d’une affection rare appelée «syndrome de fuite capillaire» qui provoque une fuite du sang des petits vaisseaux sanguins dans votre corps et nécessite une prise en charge médicale urgente.
Très fréquent (concerne plus d’un utilisateur sur 10)
– douleur osseuse. Votre médecin vous indiquera ce que vous pouvez prendre pour soulager la douleur osseuse.
Fréquent (concerne 1 à 10 utilisateurs sur 100)
– douleurs et rougeur au site d’injection, des maux de tête, des troubles généraux et des douleurs au niveau des articulations, des muscles, du thorax, des membres, du cou ou du dos.
– certaines modifications sanguines peuvent être détectées à l’occasion d’examens sanguins de routine. Le nombre de globules blancs peut augmenter pendant une courte durée de temps. Le nombre de thrombocytes (plaquettes) peut diminuer et entraîner des ecchymoses.
Occasionnel (concerne 1 à 10 utilisateurs sur 1000)
– nausées, atteinte des minuscules filtres des reins (glomérulonéphrite).
– crachat de sang (hémoptysie).
– maladies du sang (syndrome myélodysplasique [SMD] ou leucémie myéloïde aiguë [LMA]).
Rare (concerne 1 à 10 utilisateurs sur 10 000)
– symptômes de réactions allergiques au pegfilgrastim, incluant rougeur cutanée, éruptions cutanées, zones cutanées surélevées avec démangeaisons ainsi qu’anaphylaxie (faiblesse, chute de tension, difficultés respiratoires, gonflement du visage).
– problèmes respiratoires ont été signalés après l’administration de facteurs de croissance granulocytaire (G-CSF). En cas de toux, de fièvre ou de difficultés respiratoires, veuillez en informer votre médecin.
– un syndrome de Sweet (lésions douloureuses et enflées de couleur violette au niveau des membres et parfois de la face et du cou, accompagnées de fièvre). D’autres facteurs peuvent également y jouer un rôle.
– inflammation de l’aorte (le grand vaisseau sanguin qui achemine le sang du cœur dans le corps) (voir rubrique «Quelles sont les précautions à observer lors de l’utilisation de Fulphila ?»).
– saignement au niveau des poumons (hémorragie pulmonaire).
– syndrome de Stevens-Johnson, qui peut apparaître sous la forme de taches rougeâtres ressemblant à une cible ou de taches circulaires présentant souvent des cloques en leur centre et situées sur le tronc, d’une desquamation de la peau et d’ulcérations au niveau de la bouche, de la gorge, du nez, des parties génitales et des yeux, et qui peut être précédé de fièvre ou de symptômes s’apparentant à ceux de la grippe. Si l’un de ces symptômes apparaît, il convient de cesser d’utiliser Fulphila et de consulter immédiatement un médecin. Voir aussi rubrique «Quelles sont les précautions à observer lors de l’utilisation de Fulphila ?».
Très rare (concerne moins d’un utilisateur sur 10 000)
– augmentation de la taille de la rate et de rupture de la rate (fissures) après l’administration de pegfilgrastim. Quelques cas de rupture de la rate ont eu une issue fatale. C’est la raison pour laquelle il est très important que vous contactiez immédiatement votre médecin traitant si vous présentez des douleurs abdominales hautes à gauche ou des douleurs dans l’épaule gauche, car ces douleurs peuvent être le signe d’un problème de rate.
– vascularite cutanée (inflammation des vaisseaux sanguins de la peau) chez les patients recevant du pegfilgrastim.
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Conserver au réfrigérateur (à 2 °C–8 °C).
Vous pouvez sortir Fulphila du réfrigérateur et le laisser à température ambiante (sans dépasser +30 °C) pendant une durée maximale de trois jours. Dès qu’une seringue préremplie est sortie du réfrigérateur et qu’elle a atteint la température ambiante (sans dépasser +30 °C), elle doit être utilisée dans les 3 jours ou être éliminée.
Ne pas congeler.
Il est possible d’utiliser Fulphila s’il a été congelé accidentellement pendant une période unique de moins de 24 heures.
Conserver dans l’emballage d’origine, pour le protéger de la lumière.
Conserver hors de portée des enfants.
Remarques complémentaires
Remarques concernant la manipulation:
N’utilisez pas Fulphila si vous constatez que la solution est trouble ou qu’elle contient des particules. Ne pas agiter Fulphila de façon excessive, cela pourrait altérer son effet.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Fulphila ?
Solution injectable en seringue préremplie.
1 seringue préremplie contient:
Principes actifs
Pegfilgrastim 6 mg (dans 0,6 ml de solution injectable).
Le pegfilgrastim est produit à partir de bactéries E. coli génétiquement modifiées.
Excipients
Sorbitol (E420), polysorbate 20 (le polysorbate 20 peut être fabriqué avec du maïs génétiquement modifié), acide acétique, hydroxide de sodium, eau pour préparations injectables.
Numéro d’autorisation
67478 (Swissmedic)
Où obtenez-vous Fulphila ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, seulement sur ordonnance médicale non renouvelable.
Chaque emballage contient 1 seringue préremplie de 0,6 ml de solution injectable.
Les seringues préremplies comportent un système de sécurité automatique de l’aiguille et sont disponibles sous plaquette thermoformée.
Titulaire de l’autorisation
Medius AG, 4132 Muttenz
Cette notice d’emballage a été vérifiée pour la dernière fois en juillet 2021 par l’autorité de contrôle des médicaments (Swissmedic).
Instructions d’utilisation
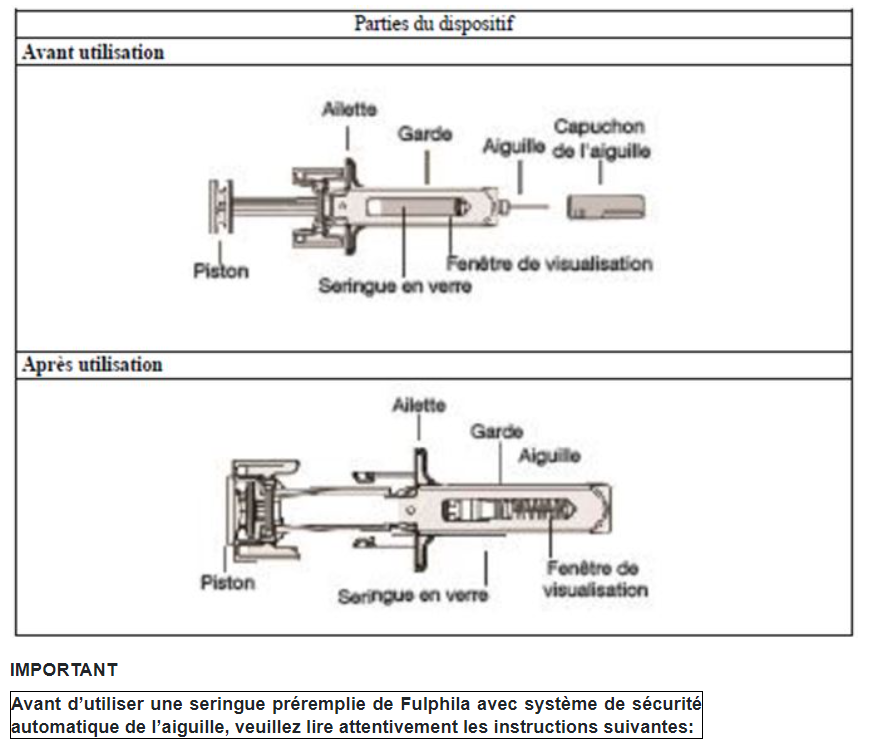
– Il est important de ne pas essayer de procéder vous-même à l’injection avant que votre médecin ou un professionnel de santé ou votre pharmacien ne vous ait montré comment faire.
– Fulphila est administré par injection dans le tissu situé juste sous la peau (injection sous-cutanée).
Pour une injection plus confortable, laissez la seringue préremplie à température ambiante pendant environ 30 minutes avant l’injection. Lavez-vous soigneusement les mains à l’eau et au savon.
Placez la seringue préremplie et le matériel nécessaire sur une surface propre et bien éclairée.
X N’essayez pas de réchauffer la seringue préremplie en utilisant une source de chaleur ou le four à micro-ondes.
X Ne laissez pas la seringue préremplie exposée directement au soleil.
X N’agitez pas la seringue préremplie.
– Tenez les seringues préremplies hors de la vue et de la portée des enfants.
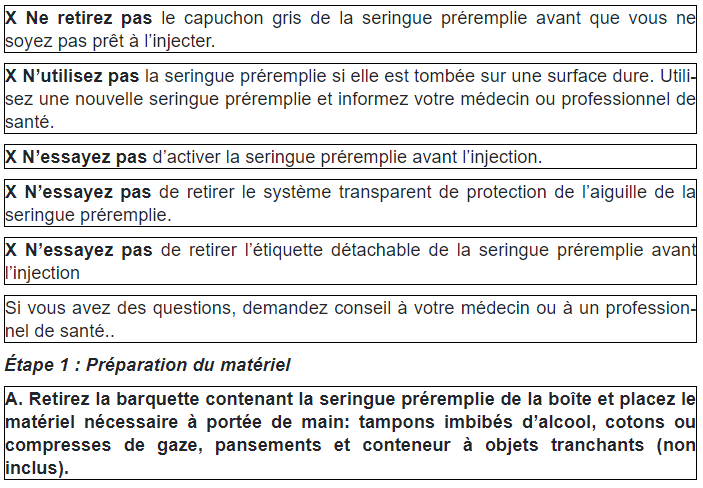
B. Ouvrez la barquette, en ôtant la pellicule de couverture. Pour retirer la seringue préremplie de la barquette, saisissez-la par le système de protection de l’aiguille.
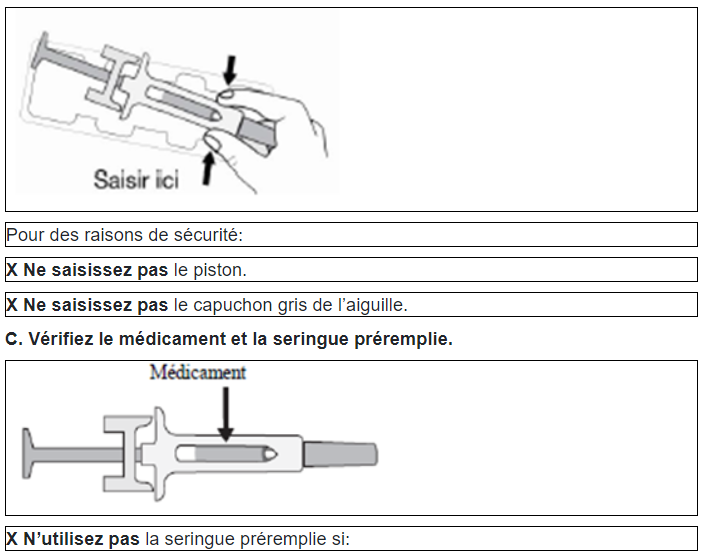
– Le produit est trouble ou s’il contient des particules. Le liquide doit être limpide et incolore.
– Une partie du dispositif apparait fissurée ou cassée.
– Le capuchon gris de l’aiguille a été retiré ou n’est pas correctement fixé.
– La date de péremption imprimée sur l’étiquette a dépassé le dernier jour du mois indiqué.
Dans tous les cas, contactez votre médecin ou un professionnel de santé.
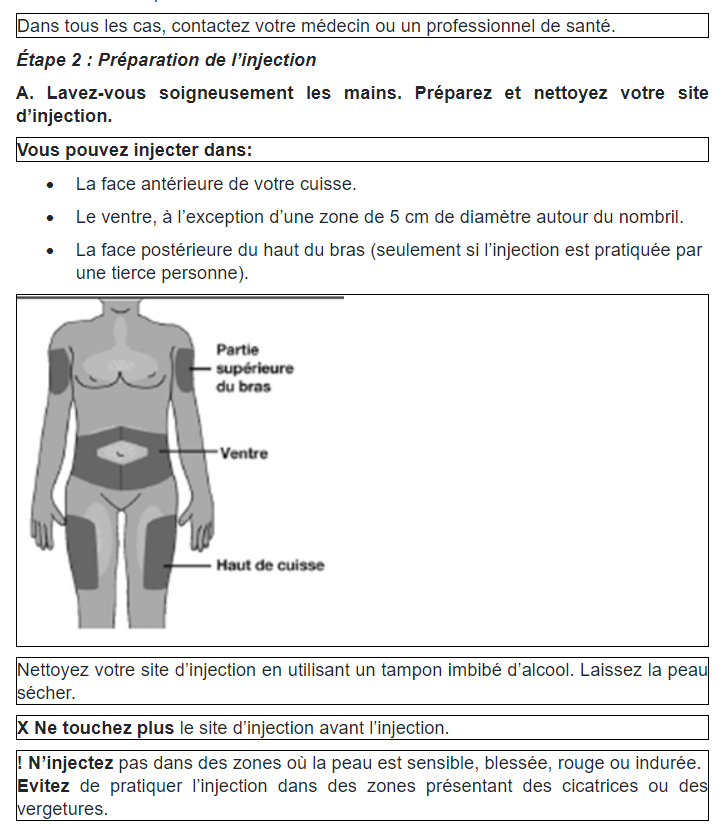
B. Retirez précautionneusement le capuchon gris dans l’axe de l’aiguille et à distance de votre corps.
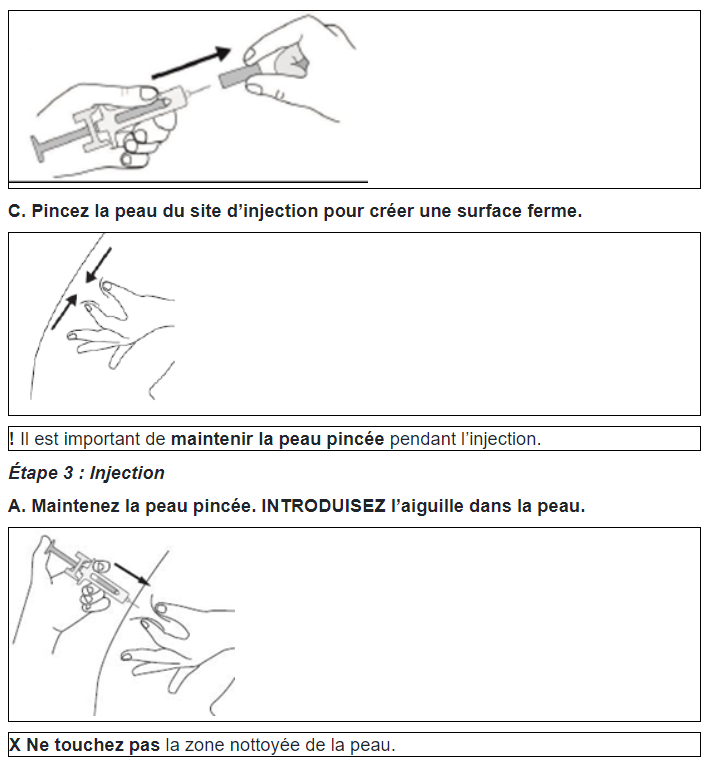
B. POUSSEZ le piston doucement et avec une pression constante, jusqu’à sentir ou entendre un «clic». Poussez le piston jusqu’au bout après le clic.

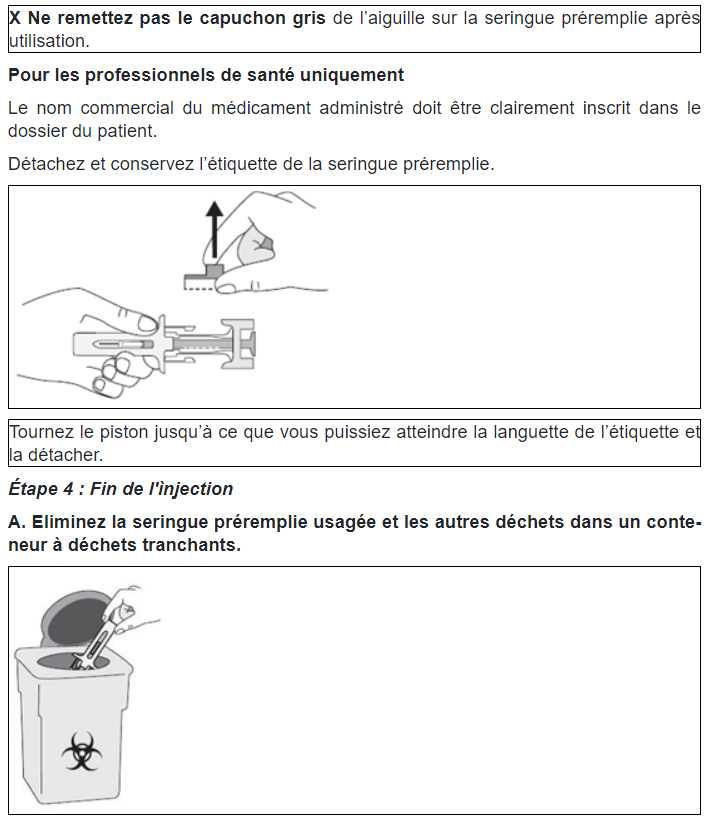
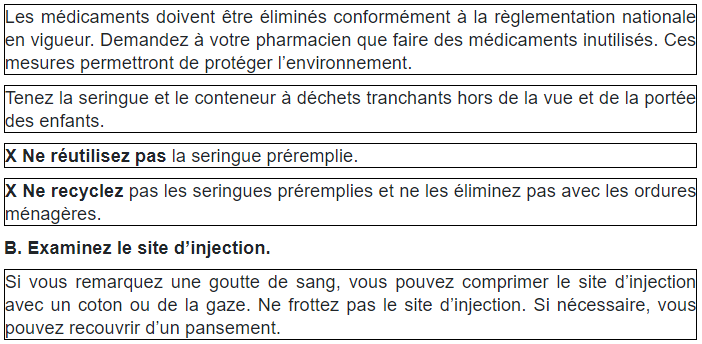
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 27.11.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans un paragraphe en gras ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 2ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (avril 2022).
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


