Glatiramyl 40 mg/ml, solution injectable en seringue préremplie
Information destinée aux patients en Suisse
Qu’est-ce que Glatiramyl 40 mg/ml et quand doit-il être utilisé ?
Selon prescription du médecin.
Glatiramyl est un médicament indiqué pour le traitement des formes récurrentes de la sclérose en plaques (SEP). Glatiramyl 40 mg/ml est utilisé pour réduire la fréquence des poussées de SEP.
Aucune efficacité n’a été prouvée sur les formes de SEP qui n’évoluent pas ou peu en poussées – en raison de leur stade avancé – ou qui évoluent avec poussées superposées.
Le principe actif de Glatiramyl est l’acétate de glatiramère, un polypeptide synthétique (agent protéique) se composant de 4 acides aminés naturels: l’acide L-glutamique, la L-alanine, la L-tyrosine et la L-lysine.
Glatiramyl est injecté par voie sous-cutanée (sous la peau) par les patients eux-mêmes.
De quoi faut-il tenir compte en dehors du traitement ?
Avant le début du traitement, assurez-vous que vous avez compris toutes les informations concernant Glatiramyl 40 mg/ml. En cas de doute, demandez à votre médecin.
N’utilisez Glatiramyl 40 mg/ml qu’après avoir été exactement informé(e) de la technique d’auto-injection par un professionnel.
Glatiramyl 40 mg/ml est destiné exclusivement à une injection sous-cutanée (sous la peau).
Quand Glatiramyl 40 mg/ml ne doit-il pas être utilisé ?
En cas d’hypersensibilité connue à l’acétate de glatiramère ou au mannitol (excipient dans Glatiramyl 40 mg/ml), Glatiramyl 40 mg/ml ne doit pas être utilisé.
Quelles sont les précautions à observer lors de l’utilisation de Glatiramyl 40 mg/ml ?
La seule voie d’administration recommandée est l’injection sous la peau.
Votre médecin vous montrera la technique d’auto-injection. Votre médecin ou un autre professionnel vous surveillera lors de la première auto-injection et pendant les 30 minutes qui suivront au début du traitement ou en cas de reprise du traitement.
Dans les minutes qui suivent l’injection de Glatiramyl 40 mg/ml, des réactions comportant au moins l’un des symptômes suivants peuvent survenir: dilatation vasculaire, douleurs dans la poitrine, difficultés respiratoires, palpitations cardiaques ou accélération du rythme cardiaque. La plupart de ces réactions disparaissent rapidement. Si une réaction ne disparait pas ou si un autre effet indésirable grave survient, vous devez consulter immédiatement votre médecin ou un médecin urgentiste et arrêter le traitement par Glatiramyl 40 mg/ml.
Si vous souffrez déjà d’une maladie cardiaque ou rénale, vous devez en informer votre médecin, car, dans ce cas, il demandera probablement de vous soumettre à des examens et à des tests réguliers.
Dans de rares cas, des lésions hépatiques graves ou une aggravation de problèmes hépatiques préexistants peuvent survenir au cours du traitement par Glatiramyl (y compris une insuffisance hépatique, une inflammation hépatique avec jaunisse et, dans des cas isolés, une transplantation hépatique). Contactez immédiatement votre médecin si vous présentez l’un des symptômes suivants: nausées, perte d’appétit, vomissements répétés, démangeaisons diffuses, urine de couleur foncée et selles claires, jaunissement de la peau ou du blanc des yeux, tendance accrue aux saignements. Avant de commencer et pendant le traitement, votre médecin effectuera régulièrement des analyses de laboratoire. Si une augmentation de certaines enzymes hépatiques (appelées transaminases) est détectée dans votre sang, il vous surveillera attentivement afin de déceler une éventuelle atteinte hépatique.
Des réactions d’hypersensibilité sérieuses (par ex. contractions violentes des muscles respiratoires, réactions allergiques sévères ou urticaire) ainsi que des cas de convulsions (crise d’épilepsie) ont également été rapportés. En cas de réaction grave, vous devez en informer immédiatement votre médecin et arrêter le traitement par Glatiramyl 40 mg/ml.
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie
– vous êtes allergique
– vous prenez déjà d’autres médicaments ou utilisez déjà d’autres médicaments en usage interne ou externe (même en automédication!).
Glatiramyl 40 mg/ml peut-il être utilisé pendant la grossesse ou l’allaitement ?
Si vous êtes enceinte, si vous supposez être enceinte ou si vous envisagez une grossesse, demandez conseil à votre médecin et demandez-lui de contrôler le traitement par Glatiramyl pendant la grossesse.
Des données limitées obtenues chez l’homme n’ont démontré aucun effet négatif d’acétate de glatiramère sur les nouveau-nés/enfants allaités.
Consultez votre médecin traitant pour confirmer que vous pouvez utiliser Glatiramyl pendant l’allaitement.
Comment utiliser Glatiramyl 40 mg/ml ?
Lors de l’utilisation de Glatiramyl 40 mg/ml, suivez toujours exactement les instructions de votre médecin.
En cas de doute, demandez conseil à votre médecin ou à votre pharmacien.
Chez les adultes, la dose est de 40 mg de Glatiramyl (1 seringue préremplie) administrée sous forme d’injection sous la peau trois fois par semaine à 48 heures d’intervalle minimum. Il est recommandé d’administrer le médicament les mêmes jours chaque semaine.
Glatiramyl 40 mg/ml ne doit pas être utilisé chez les enfants et les adolescents de moins de 18 ans.
Il est très important d’injecter correctement Glatiramyl 40 mg/ml:
– Exclusivement dans le tissu sous la peau (voie sous-cutanée) (voir ci-dessous «Instructions pour la réalisation de l’injection»)
– À la posologie prescrite par le médecin. N’utilisez que la quantité indiquée par le médecin.
– N’utilisez chaque seringue qu’une seule fois. Les restes de médicament non utilisé et les déchets doivent être jetés.
– Le contenu des seringues préremplies de Glatiramyl 40 mg/ml ne doit pas être mélangé ou injecté simultanément avec d’autres médicaments ou d’autres substances.
– N’utilisez pas la solution si elle contient des particules. Utilisez dans ce cas une autre seringue préremplie.
Si vous utilisez Glatiramyl 40 mg/ml pour la première fois, vous devez apprendre la technique d’auto-injection auprès d’un médecin ou un autre membre du personnel médical. Afin de garantir l’absence de problème, vous réaliserez votre première injection sous la surveillance du personnel médical et resterez ensuite en observation pendant 30 minutes.
L’utilisation et la sécurité de Glatiramyl 40 mg/ml n’ont pas été établies à ce jour pour les enfants de moins de 18 ans.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte. N’arrêtez jamais le traitement sans l’autorisation de votre médecin.
Si vous oubliez une injection, réalisez-la aussitôt que vous vous apercevez de votre oubli. Ne réalisez l’injection suivante que 48 heures plus tard au minimum. Ne réalisez donc pas d’injection supplémentaire pour compenser la dose oubliée. Si possible, reprenez votre schéma d’administration habituel dans la semaine suivante.
Lisez attentivement les instructions suivantes avant d’utiliser Glatiramyl pour la première fois et respectez les figures correspondantes.
Instructions pour la réalisation de l’injection
Lisez attentivement l’intégralité de ces instructions avant d’utiliser Glatiramyl.
Avant d’effectuer l’injection, assurez-vous d’avoir le médicament et tout le matériel nécessaire:
– Une seringue préremplie de Glatiramyl dans sa plaquette.
– Un tampon imbibé d’alcool (non inclus dans l’emballage).
– Le récipient destiné à la récupération des seringues usagées.
– Pour chaque injection, ne sortez de l’emballage qu’une seule plaquette contenant une seringue préremplie. Laissez les autres seringues dans la boîte.
– Si votre seringue a été conservée au réfrigérateur, sortez la plaquette contenant la seringue au moins 20 minutes avant l’injection afin que la solution atteigne la température ambiante.
Lavez-vous soigneusement les mains à l’eau et au savon.
Choisissez un site d’injection adéquat se situant dans les zones, selon les schémas.
Vous disposez de sept zones possibles où injecter le médicament:
Zone 1: Région de l’abdomen (ventre) autour du nombril. Évitez d’injecter à moins de 5 cm autour du nombril,
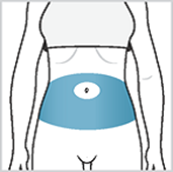
Zone 2 et 3: Cuisses (au-dessus du genou),

Zone 4, 5, 6 et 7: Arrière de la partie supérieure des bras et partie supérieure des hanches (en dessous de la taille),
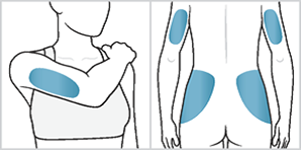
Chaque zone d’injection comporte plusieurs sites d’injection. Choisissez tous les jours un site d’injection différent afin de réduire le risque d’irritation ou de douleur au site d’injection. Alternez les zones d’injection et alternez également les sites d’injection dans une même zone. N’utilisez pas le même site à chaque fois.
Remarque: N’injectez pas à un endroit qui est douloureux, rougi, gonflé ou qui comporte une induration.
Il est recommandé de respecter un ordre planifié de rotation des sites d’injection et de noter les sites utilisés dans un agenda. Vous aurez peut-être plus de difficultés à injecter dans certaines zones de votre corps (comme la partie arrière de vos bras). Le cas échéant, vous pourriez avoir besoin d’aide.
Comment réaliser l’injection
– Nettoyez le site d’injection choisi avec un tampon imbibé d’alcool non usagé.
– Attendez 10 secondes afin de laisser sécher la peau avant de procéder à l’injection.
– Retirez la seringue de son emballage de protection en décollant le film qui recouvre la plaquette.
– Retirez l’embout de protection de l’aiguille, ne retirez pas l’aiguille avec votre bouche ou avec vos dents.
– Formez un pli au niveau de la peau en pinçant doucement la peau entre le pouce et l’index (Fig. 1).
– Insérez l’aiguille dans le pli de la peau (Fig. 2).
– Injectez la solution en enfonçant le piston de manière régulière jusqu’à ce que la seringue soit vide.
– Enlevez d’une manière droite la seringue et l’aiguille.
– Jetez la seringue dans le récipient de récupération des déchets. Ne jetez pas les seringues usagées dans les ordures ménagères, mais dans le récipient spécifique résistant à la perforation, selon la recommandation de votre médecin ou du personnel médical.
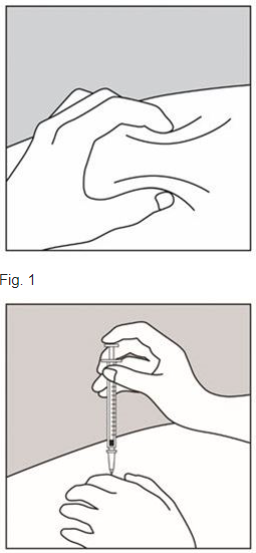
Fig. 2
Quels effets secondaires Glatiramyl 40 mg/ml peut-il provoquer ?
Des réactions au site d’injection ont représenté les effets secondaires les plus fréquemment rapportés. Les réactions locales les plus fréquentes ont été les suivantes: rougeur de la peau, douleur, formation de vésicules, démangeaisons, rétention d’eau dans les tissus, inflammation et hypersensibilité au site d’injection.
Les réactions suivantes peuvent apparaitre dans les minutes suivant l’utilisation: dilatation vasculaire (rougeur cutanée sur la poitrine ou au visage), douleur dans la poitrine, difficultés respiratoires, palpitations cardiaques ou accélération du rythme cardiaque.
Dans la plupart des cas, ces événements sont passagers. Ils disparaissent sans traitement et ne laissent pas de séquelles. Ces effets secondaires peuvent apparaître au début du traitement ou après plusieurs mois. Ils peuvent apparaître une ou plusieurs fois.
En outre, les effets secondaires suivants peuvent survenir:
Très fréquent (concerne plus d’un utilisateur sur 10)
– Infections, grippe;
– Maux de tête;
– Angoisse, dépression;
– Dilatation des vaisseaux;
– Difficultés respiratoires;
– Nausées;
– Eruptions cutanées;
– Douleurs articulaires, douleurs dorsales;
– Epuisement, douleurs dans la poitrine, réactions au site d’injection, douleur.
Fréquent (concerne 1 à 10 utilisateur sur 100)
– Bronchite;
– Troubles fonctionnels du rectum, constipation, caries dentaires, troubles digestifs, troubles de la déglutition, incontinence fécale, vomissements;
– Gastro-entérite, vésicules herpétiques, otite moyenne, rhume, abcès dentaire, infection fongique vaginale;
– Excroissance cutanée bénigne, néoformation tissulaire;
– Hypersensibilité;
– Gonflement des ganglions lymphatiques;
– Manque d’appétit, prise de poids;
– Nervosité;
– Troubles du goût, augmentation de la contraction musculaire de type crampes, migraine, trouble de l’élocution, perte de conscience, tremblements;
– Vision double, troubles fonctionnels oculaires;
– Palpitations cardiaques et augmentation du rythme cardiaque;
– Douleurs dans les oreilles;
– Toux, rhume des foins;
– Résultats anormaux des tests de la fonction hépatique;
– Saignement cutané sur une faible surface, sudation, démangeaisons, troubles cutanés, urticaire;
– Douleurs dans la nuque;
– Miction impérieuse, mictions fréquentes, rétention d’urine;
– Grelottements, gonflement du visage, atrophie tissulaire au site d’injection, réactions locales, rétentions d’eau, fièvre.
Occasionnel (concerne 1 à 10 utilisateurs sur 1000)
– Abcès, cellulite, furoncle, zona, pyélonéphrite;
– Cancer de la peau;
– Modification du nombre et de la forme des globules blancs, augmentation du volume de la rate, diminution du nombre des plaquettes sanguines;
– Réaction allergique sévère;
– Augmentation du volume de la thyroïde, hyperthyroïdie;
– Intolérance à l’alcool, goutte, augmentation des lipides sanguins, modification du sang (augmentation du taux de sodium, diminution du taux de fer);
– Rêves inhabituels, confusion, euphorie, confusion des sens, agressivité, comportement maniaque, troubles de la personnalité, tentative de suicide;
– Engourdissement et sensation douloureuse dans la main, troubles mentaux, convulsions, troubles de l’écriture, troubles de la lecture, troubles des mouvements, tressaillement musculaires, inflammations nerveuses, tétanie musculaire, mouvements oculaires, paralysie, steppage du pied, stupeur, troubles du champ visuel, troubles de l’élocution;
– Opacification du cristallin (cataracte), lésions dans la cornée, sécheresse oculaire, saignement oculaire, affaissement de la paupière, dilatation des pupilles, endommagement du nerf optique;
– Troubles du rythme cardiaque (battements cardiaques supplémentaires, fréquence cardiaque ralentie ou soudainement accélérée);
– Varices;
– Arrêt de la respiration, sensation d’étouffement, saignement de nez, accélération de la respiration, sensation d’étroitesse dans la gorge, troubles de la respiration;
– Inflammation du côlon, inflammation de l’intestin grêle, polypes dans le côlon, renvois, ulcère dans l’œsophage, inflammation des gencives, saignement rectal, augmentation du volume des glandes salivaires;
– Calculs biliaires, augmentation du volume du foie;
– Gonflement de la peau et/ou des muqueuses (angioœdème), eczéma de contact sur la peau, nodules cutanés, érythème noueux;
– Inflammation des articulations (arthrite ou ostéoarthrite), bursite, douleurs abdominales latérales, diminution de la masse musculaire;
– Sang dans les urines et troubles de l’appareil urinaire, calculs rénaux anomalies urinaires;
– Gonflement des seins, troubles de l’érection, affaissement du plancher pelvien, érection permanente, anomalie du frottis cervical, troubles des organes génitaux féminins externes, troubles fonctionnels du vagin, des testicules et de la prostate, saignements vaginaux;
– Kyste, sensation de veisalgie, température corporelle basse, inflammations non spécifiques, destruction tissulaire (nécrose) au site d’injection, troubles des muqueuses;
– Troubles après une vaccination.
Rare (concerne 1 à 10 utilisateurs sur 10’000)
– Lymphome à cellules T;
– Insuffisance cardiaque aiguë;
– Lésions hépatiques graves (y compris insuffisance hépatique et inflammation du foie (hépatite) avec jaunisse).
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Conserver au réfrigérateur (2-8°C).
Ne pas congeler. Les seringues préremplies qui ont été congelées doivent être détruites.
Conserver le récipient dans son carton pour le protéger de la lumière.
Tenir hors de portée des enfants.
Lorsqu’une conservation au réfrigérateur n’est pas possible, les seringues préremplies peuvent être conservées une seule fois jusqu’à un mois entre 15-25°C.
Les seringues préremplies qui n’ont pas été utilisées au cours de ce mois unique et qui se trouvent encore dans l’emballage original doivent être conservées au réfrigérateur ensuite.
Remarques complémentaires
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Une seringue préremplie ne doit être utilisée qu’une seule fois.
Que contient Glatiramyl 40 mg/ml ?
La seringue préremplie contient 1 ml de solution injectable prête à l’emploi.
Principes actifs
1 ml de solution contient 40 mg d’acétate de glatiramère (corresponde à 36 mg de glatiramère)
Excipients
Mannitol, eau pour préparations injectables
Numéro d’autorisation
67526 (Swissmedic)
Où obtenez-vous Glatiramyl 40 mg/ml ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Présentation: 12 seringues préremplies en emballage blister
Titulaire de l’autorisation
Viatris Pharma GmbH, Steinhausen
Cette notice d’emballage a été vérifiée pour la dernière fois en février 2022 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 06.10.2023, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 3ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (novembre 2021). Mise à jour 2 (février 2023).
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


