Rebif® RebiDose
Information destinée aux patients en Suisse
Qu’est-ce que Rebif RebiDose et quand doit-il être utilisé ?
La sclérose en plaques est une maladie affectant le système nerveux central. Son origine n’est pas encore clairement établie, mais on suppose qu’elle est liée à une réaction anormale du système immunitaire.
Les interférons sont fabriqués par l’organisme et jouent un rôle essentiel dans le système immunitaire. Par des mécanismes qui n’ont pas encore été entièrement élucidés, ils contribuent à limiter les effets de la sclérose en plaques sur le système nerveux central.
Rebif appartient à la classe des interférons. Son principe actif est l’interféron bêta-1a produit par génie génétique dans des cellules animales.
Rebif est indiqué dans le traitement de la sclérose en plaques évoluant par poussées. Il a été démontré que ce médicament réduit le nombre et la gravité des poussées et ralentit la progression du handicap. Par ailleurs, Rebif peut également être utilisé par des patients qui présentent pour la première fois des symptômes indiquant un risque élevé de développer une sclérose en plaques.
Avant de commencer le traitement, votre médecin exclura toute autre cause possible de vos troubles.
Ce médicament vous a été prescrit personnellement; vous ne devez pas le donner à une autre personne.
Ce médicament ne doit être utilisé que sur prescription du médecin.
De quoi faut-il tenir compte en dehors du traitement ?
Le médecin décide du traitement approprié à chaque patient. Suivez scrupuleusement ses indications.
Quand Rebif RebiDose ne doit-il pas être utilisé ?
Rebif ne doit pas être utilisé en cas d’allergie ou d’hypersensibilité au principe actif ou à l’un des excipients du médicament.
Rebif ne doit pas être utilisé chez des patients ayant des troubles dépressifs sévères et/ou des idées suicidaires.
Quelles sont les précautions à observer lors de l’utilisation de Rebif RebiDose ?
Rebif ne doit être utilisé que sous la surveillance de votre médecin. L’expérience relative à l’utilisation de Rebif chez les enfants et les adolescents âgés de 2 à 17 ans est limitée. Les patients de moins de 2 ans ne doivent pas utiliser Rebif, car le médicament n’a pas été suffisamment étudié dans ce groupe de patients.
Veuillez informer votre médecin si vous souffrez d’une maladie de la moelle osseuse, d’une affection de la thyroïde ou de problèmes rénaux ou hépatiques, ou si vous avez eu des crises épileptiques dans le passé. Si c’est le cas, votre médecin doit surveiller plus étroitement votre traitement et effectuer des examens sanguins à intervalles réguliers.
Adressez-vous immédiatement à votre médecin si vous avez des pensées dépressives ou suicidaires.
Prévenez votre médecin en cas de maladie du cœur. Votre médecin doit alors surveiller plus étroitement votre traitement.
Pour éviter des réactions indésirables au site d’injection, suivez minutieusement les instructions (voir sous Comment utiliser Rebif RebiDose ?).
Adressez-vous à votre pharmacien ou à votre médecin en cas de problèmes.
Ne modifiez pas le dosage ou le schéma thérapeutique de votre propre chef.
N’arrêtez pas le traitement sans consulter votre médecin. Prévenez votre médecin en cas d’allergie ou d’hypersensibilité à d’autres médicaments.
Des caillots de sang pourraient se former dans les petits vaisseaux sanguins durant votre traitement. Ces caillots de sang pourraient atteindre vos reins. Cela pourrait se manifester après plusieurs semaines, voire plusieurs années, de traitement par Rebif. Votre médecin pourrait décider de surveiller votre tension artérielle, votre bilan sanguin (nombre de plaquettes) et votre fonction rénal.
Rebif contient de l’alcool benzylique
Rebif contient 1.0 mg d’alcool benzylique par dose de 0.2 ml et 2.5 mg d’alcool benzylique par dose de 0.5 ml. L’alcool benzylique peut provoquer des réactions allergiques. L’alcool benzylique est associé à un risque d’effets secondaires graves y compris des problèmes respiratoires (appelés «syndrome de suffocation») chez les jeunes enfants. Il ne doit pas être administré aux prématurés ni aux nouveau-nés à terme. Il peut provoquer des réactions toxiques et des réactions allergiques chez les nourrissons et les enfants jusqu’à 3 ans.
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose (0.2 ml ou 0.5 ml), c.-à-d qu’il est essentiellement «sans sodium».
Votre aptitude à conduire ou utiliser des outils ou des machines peut être altérée par les effets de la maladie elle-même ou du traitement. Si vous êtes concerné(e), parlez-en à votre médecin.
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie
– vous êtes allergique
– vous prenez déjà d’autres médicaments (même en automédication!).
Veuillez informer votre médecin tout particulièrement si vous prenez des antiépileptiques (médicaments contre l’épilepsie) ou des antidépresseurs (médicaments contre la dépression).
Rebif RebiDose peut-il être utilisé pendant la grossesse ou l’allaitement ?
Si vous êtes enceinte ou que vous allaitez, si vous pensez être enceinte ou planifiez une grossesse, demandez conseil à votre médecin avant de prendre Rebif.
Comment utiliser Rebif RebiDose ?
Rebif est disponible sous forme de solution injectable en seringue pré-remplie, pré-assemblée dans un applicateur (stylo pré-rempli nommé «RebiDose») pour une auto-administration unique. Le stylo pré-rempli est prêt à l’emploi. Trois dosages sont disponibles: 8.8 microgrammes (stylo pré-rempli avec un bouton jaune), 22 microgrammes (stylo pré-rempli avec un bouton vert) et 44 microgrammes (stylo pré-rempli avec un bouton vert pétrole).
Dosage
Patients présentant de premiers symptômes («syndrome clinique isolé»)
La posologie recommandée chez les patients adultes est de 44 microgrammes trois fois par semaine.
Patients atteints de sclérose en plaques évoluant par poussées
Chez les adultes âgés de 18 ans et plus, la posologie recommandée est de 44 microgrammes trois fois par semaine. Rebif 22 microgrammes, également administré trois fois par semaine, est recommandé aux patients qui ne tolèrent pas la dose supérieure.
Pour plus d’informations sur la toléreance du médicament chez les enfants de 2 ans et plus et chez les adolescents, voir également «Quels effets secondaires Rebif peut-il provoquer ?»
L’utilisation de Rebif n’est pas recommandée chez les enfants de moins de 2 ans.
Les injections doivent être administrées autant que possible au même moment de la journée (le soir de préférence), les 3 mêmes jours de la semaine (en respectant un intervalle d’au moins 48 heures).
Il est possible de ne pas remarquer les effets de Rebif immédiatement. Dans ce cas, n’interrompez pas votre traitement, mais poursuivez-le conformément aux instructions afin d’obtenir le résultat souhaité. Concernant la durée du traitement, suivez les conseils de votre médecin.
Si vous avez un doute quant aux bénéfices du traitement, veuillez consulter votre médecin.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Début du traitement
Au début du traitement par Rebif, le schéma posologique suivant est recommandé en vue de diminuer l’importance de certains effets secondaires:
Pour un dosage-cible de Rebif 44 µg trois fois par semaine:
– au cours des deux premières semaines, à chaque jour de traitement on injectera 20 % de la dose totale (c.-à-d. 8.8 µg par injection) = volume total du stylo pré-rempli de 8.8 µg (bouton jaune), trois fois par semaine;
– au cours de la troisième et de la quatrième semaine, à chaque jour de traitement on injectera 50 % de la dose totale (c.-à-d. 22 µg par injection) = volume total du stylo pré-rempli de 22 µg (bouton vert), trois fois par semaine;
– à partir de la cinquième semaine et pendant le reste de la durée du traitement, on injectera l’intégralité de la dose (c.-à-d. 44 µg par injection) = volume total du stylo pré-rempli de 44 µg (bouton vert pétrole), trois fois par semaine.
Pour un dosage-cible de Rebif 22 µg trois fois par semaine:
Au cours des quatre premières semaines, il est recommandé d’utiliser le coffret d’initiation de Rebif solution injectable en seringues pré-remplies pour procéder à l’augmentation progressive de la dose, étant donné que le stylo pré-rempli RebiDose ne permet, contrairement aux seringues pré-remplies, que d’injecter la totalité du contenu du stylo RebiDose (et non une partie du contenu):
– au cours des deux premières semaines, à chaque jour de traitement on injectera 20 % de la dose totale (c.-à-d. 4.4 µg par injection) = 0.1 ml de la seringue de 8.8 µg, trois fois par semaine;
– au cours de la troisième et de la quatrième semaine, à chaque jour de traitement on injectera 50 % de la dose totale (c.-à-d. 11 µg par injection) = 0.25 ml de la seringue de 22 µg, trois fois par semaine.
A partir de la cinquième semaine, les stylos pré-remplis à 22 µg peuvent être utilisés:
– à partir de la cinquième semaine et pendant le reste de la durée du traitement, on injectera l’intégralité de la dose (c.-à-d. 22 µg par injection) = volume total du stylo pré-rempli de 22 µg (bouton vert), trois fois par semaine.
Instructions pour l’auto-injection
Rebif doit être administré par voie sous-cutanée (sous la peau).
La première injection doit être effectuée en présence d’une personne qualifiée en la matière.
Votre médecin traitant ou le personnel soignant vous instruira et vous aidera à acquérir la technique de l’auto-injection. Recourez à cette aide aussi longtemps que nécessaire pour maîtriser complètement la technique et l’exécution de l’auto-injection. Comme Rebif est disponible en stylo pré-rempli RebiDose pour administration sous-cutanée, vous ou un membre de votre famille ou un ami pouvez réaliser l’injection.
Pour l’administration de Rebif à l’aide du stylo pré-rempli RebiDose, lisez attentivement les instructions suivantes et suivez-les point par point:
Choix d’un site d’injection
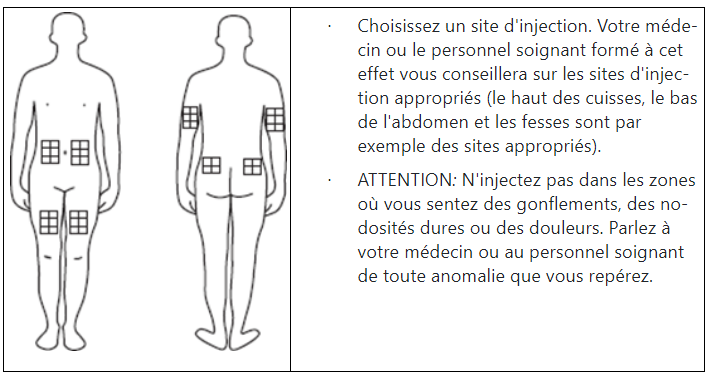
Changement du site d’injection
Par la rotation régulière du site d’injection, vous pouvez éviter des réactions au site d’injection. Vous laissez ainsi au site utilisé le temps de se remettre. L’injection du jour ne doit pas être effectuée au même site que celui de la précédente injection.
Notez où et quand vous avez procédé aux dernières injections. On peut par exemple noter ces données sur un calendrier mensuel.
Un site d’injection peut être de nouveau utilisé après environ une semaine. Si tous les sites d’injection deviennent douloureux, consultez votre médecin pour déterminer d’autres sites d’injection.
Si vous éprouvez des difficultés à atteindre l’un ou l’autre des sites d’injection, demandez de l’aide à votre infirmier ou à une personne expérimentée dans la technique d’injection.
Préparation de l’injection sous-cutanée
Ce médicament est destiné à un usage unique. N’utilisez chaque stylo pré-rempli RebiDose qu’une seule fois:
– Sortez le stylo pré-rempli du réfrigérateur au moins 30 minutes avant l’injection.
– Lavez-vous soigneusement les mains à l’eau et au savon;
Dès que vous avez choisi un site d’injection
– Rassemblez tous les accessoires dont vous avez besoin et placez-les sur une surface propre: un stylo pré-rempli «RebiDose» neuf, un tampon imprégné d’alcool, un tampon sec ou une gaze en coton.
– Sortez le stylo pré-rempli de son emballage blister en enlevant la feuille plastique;
– Vérifiez l’aspect de Rebif à travers la fenêtre de contrôle transparente. La solution doit être limpide à opalescente; il ne doit y avoir aucune particule, ni aucun signe visible de dégradation. Si des particules ou signes visibles de dégradation sont présents, n’utilisez pas Rebif et informez-en votre médecin, votre infirmier ou votre pharmacien;
– Contrôlez la date de péremption indiquée sur l’étiquette du stylo pré-rempli RebiDose ou sur l’emballage en carton. Si la date de péremption est dépassée, le stylo pré-rempli RebiDose ne doit plus être utilisé.
L’image ci-après illustre l’aspect du stylo pré-rempli RebiDose en détail:

Comment injecter Rebif RebiDose ?
– Avant l’injection, nettoyez la peau au niveau du site d’injection à l’aide d’un tampon d’alcool. Laissez sécher la peau. Si de l’alcool reste sur la peau, vous pouvez ressentir une sensation de brûlure.
– Ne retirez le capuchon de protection de l’aiguille d’injection que lorsque vous êtes prêt(e) à faire l’injection.
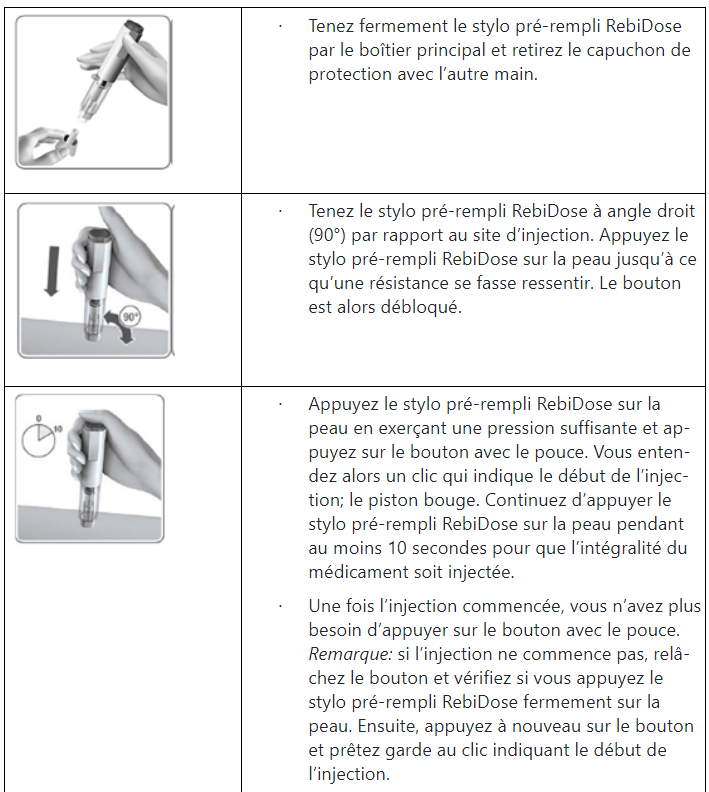

– Massez doucement le site d’injection avec un tampon sec d’ouate ou de gaze en coton.
– Ne remettez pas le capuchon de protection de l’aiguille sur le stylo pré-rempli RebiDose déjà utilisé, étant donné que l’aiguille est protégée par le dispositif de sécurité. Ne placez pas vos doigts dans l’ouverture du dispositif de sécurité.
– Rebif RebiDose est un stylo pré-rempli à usage unique et ne doit jamais être réutilisé.
– Dès que l’injection est terminée, jetez le stylo pré-rempli RebiDose dans un collecteur adéquat. Demandez à votre pharmacien comment éliminer le stylo pré-rempli RebiDose en toute sécurité.
Si vous avez utilisé une quantité de Rebif supérieure à la dose prescrite
En cas d’un surdosage, veuillez immédiatement vous adresser à votre médecin.
Si vous avez oublié d’administrer Rebif
Si vous avez oublié une dose, poursuivez les injections le jour de la prochaine dose prévue. N’injectez pas le double de la dose si vous avez oublié la précédente administration.
Si vous avez des questions supplémentaires, veuillez vous adresser à votre médecin, votre infirmier ou votre pharmacien.
Quels effets secondaires Rebif RebiDose peut-il provoquer ?
L’utilisation d’interféron bêta peut provoquer les effets secondaires suivants:
Symptômes pseudo-grippaux, tels que des maux de tête, fièvre, frissons, fatigue, nausées et douleurs musculaires et articulaires. Ces effets se manifestent en début de traitement chez 7 patients sur 10. Ils diminuent avec la poursuite du traitement. Pour soulager ces symptômes, votre médecin peut vous prescrire un analgésique, modifier temporairement le dosage ou interrompre le traitement. Vous ne devez pas arrêter ou modifier le traitement si votre médecin ne l’a pas ordonné.
Des réactions au site d’injection telles que rougeur, gonflement, changement de couleur, inflammation, douleur, lésion de la peau et destruction des tissus cutanés (nécroses) ainsi que d’autres réactions non spécifiques peuvent se produire chez environ 3 patients sur 10. La survenue des réactions au site d’injection diminue habituellement avec le temps. Si vous avez des réactions locales anormales, veuillez vous adresser à votre médecin.
D’autres effets indésirables moins fréquents associés à l’interféron bêta ont été rapportés: diarrhée, vomissement, perte d’appétit, hépatite, troubles du sommeil, vertiges, nervosité, éruption cutanée, urticaire, chute des cheveux, troubles visuels, démangeaisons, sentiment d’angoisse et palpitations.
Durant le traitement par interféron bêta, les effets secondaires suivants peuvent aussi apparaître: Altérations de la rétine entraînant des troubles visuels, pensées suicidaires, crises convulsives, réactions cutanées sévères (certaines s’accompagnant de lésions des muqueuses), difficultés respiratoires, augmentation de la transpiration, infections au site d’injection, affections du système immunitaire impliquant la peau (lupus érythémateux médicamenteux, réversible après l’arrêt du médicament), diminution du nombre de globules rouges et blancs ainsi que des plaquettes sanguines (pancytopénie), ou formation de caillots sanguins (thrombus) à l’intérieur des petits vaisseaux sanguins dans tout le corps qui pourraient atteindre vos reins (purpura thrombotique thrombocytopénique ou syndrome hémolytique et urémique). Ceci entraîne une anémie en raison d’une destruction accrue des globules rouges (anémie hémolytique) ainsi qu’une diminution du nombre de plaquettes circulantes. Les symptômes peuvent inclure une tendance accrue aux saignements (saignements sous-cutanés ainsi que petits saignements de couleur violette dans la peau (Purpura) et saignements internes), une facilité à faire des bleus, de la fièvre, une sensation extrême de faiblesse, des maux de tête, des vertiges ou des étourdissements peuvent apparaître. Votre médecin pourrait trouver des modifications de votre bilan sanguin et de votre fonction rénale. Troubles rénaux, incluant la formation de tissu cicatriciel, susceptibles d’altérer la fonction rénale. Si vous présentez l’un de ces symptômes ou tous – urine mousseuse, fatigue, gonflement, en particulier des chevilles et des paupières, et prise de poids – Informez-en votre médecin car cela pourrait être les signes d’un problème rénal.
Très rarement, des réactions allergiques graves (hypersensibilité) peuvent apparaître. Contactez immédiatement votre médecin si une détresse respiratoire ou un gonflement du visage, éventuellement aussi associés à une urticaire et à une sensation de faiblesse, surviennent soudain chez vous immédiatement après l’administration de Rebif .
En cas d’effets secondaires sévères ou persistants, veuillez consulter votre médecin.
Le nombre de globules blancs et rouges ou de plaquettes peut diminuer et les paramètres hépatiques peuvent être modifiés. C’est la raison pour laquelle votre sang devrait être analysé avant le traitement et ensuite à intervalles réguliers.
Ces changements ne sont généralement pas perçus par le patient (aucun symptôme). Ils sont habituellement réversibles et légers. Si vous remarquez néanmoins des symptômes indiquant un trouble hépatique, tels qu’une perte d’appétit associée à d’autres symptômes tels que nausées, vomissements ou jaunisse, contactez immédiatement votre médecin.
Les interférons peuvent provoquer une hyperfonction ou au contraire une insuffisance fonctionnelle de votre glande thyroïde. Ces modifications de l’activité thyroïdienne sont rarement perçues par le patient. Cependant, votre médecin peut juger nécessaire de procéder à un examen.
Une dépression et même des idées suicidaires peuvent survenir plus fréquemment chez les patients atteints de sclérose en plaques. Si vous éprouvez de tels sentiments, consultez immédiatement votre médecin.
Au début du traitement par Rebif, des symptômes ressemblant à ceux d’une pseudo-poussée de sclérose en plaques peuvent survenir. Par exemple, vos muscles peuvent sembler très lourds ou faibles, ce qui vous gêne dans vos activités quotidiennes. Dans certains cas, de tels symptômes sont associés à la fièvre ou aux symptômes pseudo-fébriles décrits plus haut.
Autres effets indésirables (fréquence inconnue – ne peut être estimée sur la base des données disponibles)
Hypertension artérielle pulmonaire: un rétrécissement important des vaisseaux sanguins dans les poumons qui entraîne une augmentation de la pression artérielle dans les vaisseaux sanguins qui transportent le sang du cœur aux poumons. L’hypertension artérielle pulmonaire a été observée à des périodes diverses du traitement, notamment jusqu’à plusieurs années après le début du traitement par Rebif.
Enfants et adolescents
Aucune étude clinique formelle n’a été menée chez les enfants ou les adolescents. Certaines données cliniques existantes indiquent cependant que le profil de sécurité chez les enfants (2 à 11 ans) et les adolescents (12 à 17 ans), traités par Rebif 22 µg ou Rebif 44 µg trois fois par semaine, est similaire au profil de sécurité constaté chez les adultes.
Rebif doit être utilisé avec prudence chez les enfants (2 à 11 ans).
Si vous remarquez des effets secondaires, veuillez en informer votre médecin, votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Le médicament doit être conservé au réfrigérateur entre 2°C et 8°C (ne pas congeler).
Conservez Rebif dans son emballage d’origine pour le protéger de la lumière.
Afin d’éviter un gel accidentel, placez toujours l’emballage à l’avant du réfrigérateur.
S’il est temporairement impossible de conserver Rebif au réfrigérateur (entre 2 et 8° C), ce médicament peut être conservé à température ambiante (jusqu’à 25° C au maximum) pendant 14 jours au maximum. Après échéance de cette période de conservation de 14 jours à température ambiante, vous devez à nouveau conserver le médicament au réfrigérateur (entre 2 et 8°C) et vous pouvez l’utiliser jusqu’à la date figurant après la mention «EXP» sur l’emballage.
Tout produit non utilisé doit être retourné à la pharmacie par mesure de précaution.
Rebif doit être conservé, comme tous les médicaments, hors de la portée des enfants.
N’utilisez pas ce produit si vous constatez des signes visibles de détérioration, comme des détériorations de l’emballage plastique du stylo pré-rempli ou du stylo pré-rempli lui-même.
Remarques complémentaires
Pour des plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Rebif RebiDose ?
Principes actifs
1 stylo pré-rempli de Rebif RebiDose de 0.2 ml contient: 8.8 microgrammes d’interféron bêta-1a ADNr (soit 2.4 millions d’U.I.)
1 stylo pré-rempli de Rebif RebiDose de 0.5 ml contient: 22 ou 44 microgrammes d’interféron bêta-1a ADNr (soit 6 millions d’U.I. ou 12 millions d’U.I.)
Excipients
1 stylo pré-rempli de Rebif RebiDose de 0.2 ml contient: mannitol, poloxamère 188, acétate de sodium trihydraté, hydroxyde de sodium, acide acétique, méthionine, alcool benzylique et eau pour préparations injectables
1 stylo pré-rempli de Rebif RebiDose de 0.5 ml contient: mannitol, poloxamère 188, acétate de sodium trihydraté, hydroxyde de sodium, acide acétique, méthionine, alcool benzylique et eau pour préparations injectables
Numéro d’autorisation
62067 (Swissmedic)
Où obtenez-vous Rebif RebiDose ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Emballages contenant:
– coffret d’initiation de traitement: 6 stylos pré-remplis de Rebif 8.8 microgrammes et 6 stylos pré-remplis de Rebif 22 microgrammes
– 12 stylos pré-remplis de Rebif 22 microgrammes
– 12 stylos pré-remplis de Rebif 44 microgrammes
Titulaire de l’autorisation
Merck (Suisse) SA, Zoug
Cette notice d’emballage a été vérifiée pour la dernière fois en mars 2024 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 24.05.2024, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


