SKYRIZI® 360 mg, solution injectable en cartouche pour dispensateur de dose
Information destinée aux patients en Suisse
Qu’est-ce que SKYRIZI 360 mg et quand doit-il être utilisé ?
SKYRIZI est utilisé sur prescription médicale pour le traitement de la maladie de Crohn modérée à sévère chez les adultes ayant présenté une réponse insuffisante, une perte de réponse ou une intolérance à d’autres médicaments.
SKYRIZI contient le principe actif risankizumab. Le médicament inhibe une protéine dans l’organisme, appelée interleukine-23 (IL-23), qui provoque des inflammations. SKYRIZI soulage l’inflammation et peut ainsi contribuer à atténuer les signes et symptômes de votre maladie comme les douleurs abdominales, la diarrhée et la fatigue, et à faciliter la cicatrisation de l’intestin, ce qui peut améliorer votre qualité de vie.
De quoi faut-il tenir compte en dehors du traitement ?
Les données relatives au traitement de la maladie de Crohn par SKYRIZI au-delà de 1 an sont limitées. Les risques à long terme liés à l’utilisation de SKYRIZI ne sont pas connus.
Suivez rigoureusement les instructions de votre médecin.
Quand SKYRIZI 360 mg ne doit-il pas être utilisé ?
SKYRIZI ne doit pas être utilisé:
– si vous êtes hypersensible (allergique) au risankizumab ou à l’un des excipients de SKYRIZI.
– si vous avez une infection active cliniquement significative (p.ex. une tuberculose active).
Quelles sont les précautions à observer lors de l’utilisation de SKYRIZI 360 mg ?
Veuillez contacter votre médecin, votre pharmacien ou le personnel infirmier avant d’utiliser SKYRIZI si:
– vous souffrez actuellement d’une infection, vous êtes sous traitement pour une infection ou vous avez une infection récurrente.
– vous pensez avoir une infection ou les symptômes d’une infection (voir ci-dessous «Prêtez attention aux infections et aux réactions allergiques»).
– vous souffrez de tuberculose (TB) ou vous avez été en contact rapproché avec une personne atteinte de TB.
– vous avez récemment été vacciné ou vous prévoyez une vaccination. Pendant le traitement par SKYRIZI, vous ne devez pas être vacciné avec certains types de vaccins.
– vous recevez ou avez précédemment reçu une photothérapie; dans ce cas, votre médecin recherchera la présence de tumeurs cutanées avant et pendant le traitement par SKYRIZI.
Si vous n’êtes pas sûr d’être concerné par l’un des facteurs ci-dessus, adressez-vous à votre médecin, votre pharmacien ou au personnel infirmier avant d’utiliser SKYRIZI.
Prêtez attention aux infections et aux réactions allergiques:
SKYRIZI peut affaiblir vos défenses immunitaires et donc augmenter votre sensibilité aux infections et le risque de réactions allergiques. Informez votre médecin ou consultez immédiatement un médecin si vous remarquez les signes d’une infection ou d’une réaction allergique pendant l’utilisation de SKYRIZI. Ces signes sont répertoriés ci-dessous:
– Infections
Fièvre ou symptômes pseudo-grippaux, douleurs musculaires, toux, essoufflement, sensation de brûlure lors des mictions ou mictions plus fréquentes que d’habitude, expectoration sanglante (mucosités), perte de poids, diarrhée ou douleurs abdominales, peau chaude, rouge ou endolorie, ou plaies sur le corps.
– Réactions allergiques
Difficultés à respirer ou à déglutir, gonflement du visage, des lèvres, de la langue ou de la gorge, fortes démangeaisons avec éruption rouge ou bosses.
Aptitude à conduire et capacité à utiliser des machines:
On ne sait pas si SKYRIZI a un effet sur l’aptitude à conduire et sur la capacité à utiliser des machines.
Ce médicament contient moins de 1 mmol de sodium (23 mg) par dose de 360 mg, c.-à-d. qu’il est pratiquement «sans sodium».
Veuillez informer votre médecin, votre pharmacien ou le personnel infirmier si
– vous souffrez d’une autre maladie
– vous êtes allergique ou
– vous utilisez ou prenez d’autres médicaments (même en automédication) ou d’autres médicaments en usage externe.
SKYRIZI 360 mg peut-il être pris pendant la grossesse ou l’allaitement ?
Grossesse
Il est préférable de renoncer à utiliser SKYRIZI pendant la grossesse, car on ne sait pas quel effet ce médicament a sur l’enfant. Si vous êtes une femme en âge de procréer, il vous sera conseillé d’éviter une grossesse et vous devrez utiliser un contraceptif efficace pendant l’utilisation de SKYRIZI et pendant au moins 20 semaines après la dernière prise de SKYRIZI. Si vous êtes enceinte, suspectez une grossesse ou envisagez une grossesse, demandez conseil à votre médecin avant d’utiliser le médicament.
Allaitement
Si vous allaitez ou vous avez l’intention d’allaiter, parlez-en à votre médecin avant d’utiliser ce médicament. Vous et votre médecin devrez décider ensemble si vous allaitez votre enfant ou si vous utilisez SKYRIZI. Il n’est pas conseillé de faire les deux.
Comment utiliser SKYRIZI 360 mg ?
Utilisez toujours ce médicament comme vous l’a indiqué votre médecin, votre pharmacien ou le personnel infirmier. Si vous avez le moindre doute concernant l’utilisation de ce médicament, demandez à votre médecin, votre pharmacien ou au personnel infirmier.
SKYRIZI est administré sous la peau (il s’agit d’une «injection sous-cutanée»).
Vous déciderez avec votre médecin, votre pharmacien ou le personnel infirmier si vous pouvez vous injecter SKYRIZI vous-même. Vous pourrez vous auto-injecter ce médicament dès que votre médecin, votre pharmacien ou le personnel infirmier vous aura appris à le faire. Les injections peuvent également vous être administrées par un accompagnateur ayant reçu une formation appropriée.
Avant de vous auto-injecter SKYRIZI, veuillez lire les «Précautions d’emploi».
Quelles sont les quantités de SKYRIZI utilisées ?
Vous avez commencé le traitement par SKYRIZI avec une dose initiale de 600 mg, que votre médecin vous a injectée par une perfusion dans le bras (perfusion intraveineuse). Votre médecin vous a à nouveau administré une dose de 600 mg par perfusion intraveineuse 4 semaines et 8 semaines après cette première dose.
Vous recevrez ensuite SKYRIZI sous forme d’injection sous-cutanée.. La dose de 360 mg est injectée à l’aide d’un dispensateur de dose 4 semaines après la dernière administration intraveineuse. 8 semaines après cette première injection sous-cutanée avec le dispensateur de dose puis toutes les 8 semaines par la suite, une dose de 360 mg est administrée avec le dispensateur de dose.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Si vous avez utilisé plus de SKYRIZI que vous auriez dû
Si vous avez utilisé plus de SKYRIZI que vous auriez dû ou si la dose a été administrée plus tôt que ce qui vous a été prescrit, parlez-en à votre médecin.
Si vous avez oublié d’utiliser SKYRIZI
Si vous avez oublié d’utiliser SKYRIZI, parlez-en à votre médecin.
Si vous arrêtez d’utiliser SKYRIZI
N’arrêtez pas d’utiliser SKYRIZI sans avoir préalablement consulté votre médecin. Si vous arrêtez le traitement, il se peut que vos symptômes réapparaissent.
Enfants et adolescents
L’utilisation et la sécurité de SKYRIZI n’ont pas été établies à ce jour pour les enfants et les adolescents.
Quels effets secondaires SKYRIZI 360 mg peut-il provoquer ?
Comme tous les médicaments, ce médicament peut également avoir des effets secondaires, bien qu’ils ne surviennent pas systématiquement chez tout le monde.
Contactez immédiatement votre médecin ou obtenez une aide médicale si vous ressentez les symptômes d’une infection sévère, notamment:
– Fièvre, symptômes pseudo-grippaux, sueurs nocturnes
– Sensation de fatigue ou d’essoufflement, toux persistante
– Peau chaude, rougie et endolorie ou éruption cutanée douloureuse accompagnée de petites vésicules
Votre médecin décidera si vous pouvez continuer à utiliser SKYRIZI.
Autres effets secondaires
Informez votre médecin, votre pharmacien ou le personnel infirmier si vous ressentez l’un des effets secondaires suivants:
Très fréquent (concerne plus d’un utilisateur sur 10)
– Infections des voies respiratoires supérieures accompagnées de symptômes tels que maux de gorge ou nez bouché
Fréquent (concerne 1 à 10 utilisateurs sur 100)
– Sensation de fatigue ou faiblesse
– Infection fongique de la peau
– Réactions au site d’injection (telles que rougeur, gonflement, bleu ou douleurs)
– Démangeaisons
– Céphalées
Occasionnel (concerne 1 à 10 utilisateurs sur 1000)
– Petites irrégularités rouges proéminentes sur la peau
Si vous remarquez des effets secondaires, veuillez en informer votre médecin, votre pharmacien ou le personnel infirmier. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Conserver au réfrigérateur (2-8 °C). Ne pas congeler.
Si besoin, vous pouvez également conserver la cartouche jusqu’à 24 heures en dehors du réfrigérateur (jusqu’à 25 °C maximum).
Conserver la cartouche dans l’emballage d’origine afin de protéger le contenu de la lumière.
Conservez ce médicament hors de portée des enfants.
Remarques complémentaires
SKYRIZI est un liquide clair et incolore à jaune présenté dans une cartouche.
Le liquide peut contenir de minuscules particules blanches ou transparentes. Ne pas utiliser si le liquide est trouble ou s’il contient des flocons ou de grosses particules.
Demandez à votre médecin, votre pharmacien ou au personnel infirmier comment mettre au rebut le matériel usagé en toute sécurité.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient SKYRIZI 360 mg ?
SKYRIZI est une solution injectable en cartouche pour dispensateur de dose.
Principes actifs
Chaque cartouche de SKYRIZI 360 mg contient 360 mg du principe actif risankizumab dans 2,4 ml de solution.
Excipients
Les autres composants présents dans la cartouche de 360 mg sont de l’acétate de sodium trihydraté, de l’acide acétique, du tréhalose dihydraté, du polysorbate 20 et de l’eau pour préparations injectables.
Numéro d’autorisation
68946 (Swissmedic)
Où obtenez-vous SKYRIZI 360 mg ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, seulement sur ordonnance médicale.
Boîte contenant 1 cartouche et 1 dispensateur de dose.
Titulaire de l’autorisation
AbbVie AG, 6330 Cham (Suisse)
Cette notice d’emballage a été vérifiée pour la dernière fois en février 2024 par l’autorité de contrôle des médicaments (Swissmedic).
Précautions d’emploi
Veuillez lire L’INTÉGRALITÉ de cette notice d’emballage (information destinée aux patients) et ces précautions d’emploi avant d’utiliser le dispensateur de dose avec la cartouche SKYRIZI 360 mg.
Dispensateur de dose pour SKYRIZI
Avant
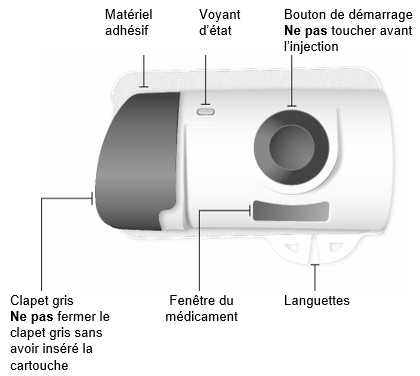
Dos
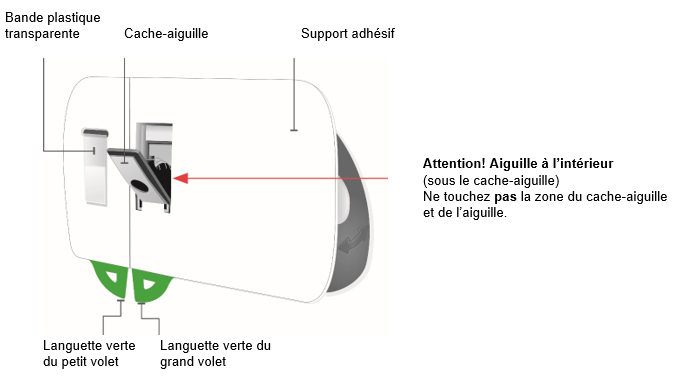
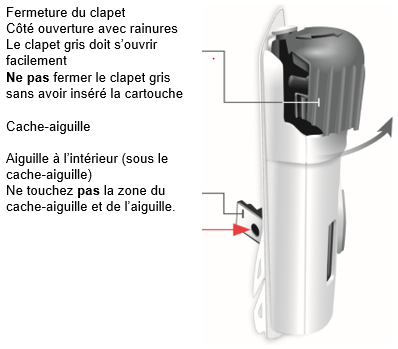
Vue latérale
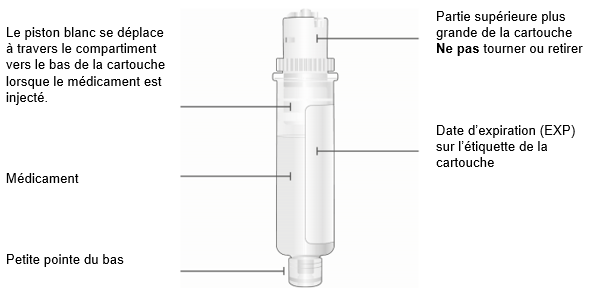
Cartouche
Ce que vous devez savoir avant l’injection de SKYRIZI
– Vous devez recevoir une formation sur la manière d’injecter SKYRIZI avant de vous administrer une injection. Parlez avec votre médecin, votre pharmacien ou votre personnel infirmier si vous avez besoin d’aide.
– Notez les dates sur votre calendrier pour savoir quand vous devez procéder à l’injection de SKYRIZI.
– Le dispensateur de dose est destiné à un usage unique et est uniquement prévu pour une utilisation avec les cartouches de SKYRIZI.
– Conservez SKYRIZI dans le carton d’origine afin de protéger le médicament de la lumière jusqu’au moment de l’utilisation.
– Sortez l’emballage du réfrigérateur et laissez-le reposer à température ambiante pendant 45 à 90 minutes, à l’abri de la lumière directe du soleil, avant l’injection.
– Le dispensateur de dose ne doit pas entrer en contact avec l’eau ou d’autres liquides.
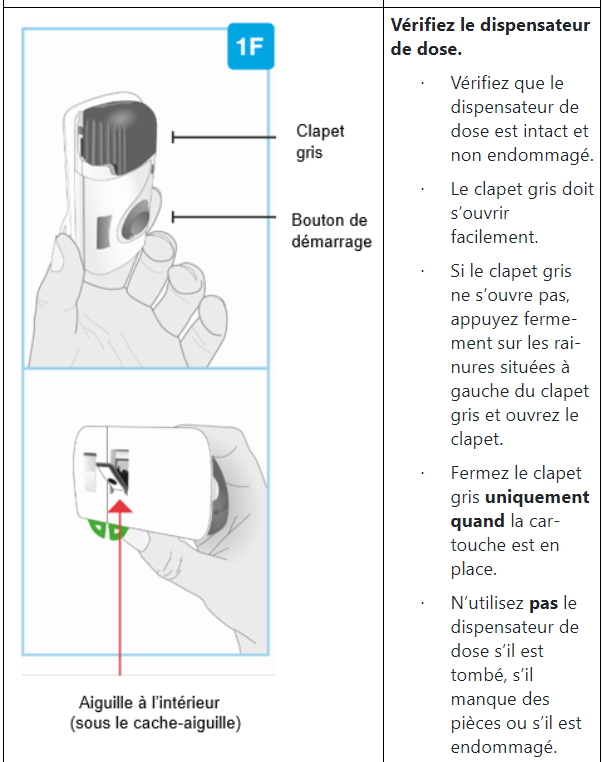
– Appuyez sur le bouton de démarrage seulement une fois que vous avez placé le dispensateur de dose avec la cartouche insérée sur la peau et que vous êtes prêt à procéder à l’injection.
– Vous ne pouvez appuyer qu’une seule fois sur le bouton de démarrage.
– Pendant le processus d’injection, l’activité physique doit être limitée. Les activités physiques modérées comme la marche, le fait de saisir quelque chose ou de se pencher sont possibles.
– Une fois que la cartouche nettoyée est insérée dans le dispensateur de dose, n’attendez pas pour injecter le médicament. Sinon, le médicament sèche et le dispensateur de dose ne peut plus fonctionner.
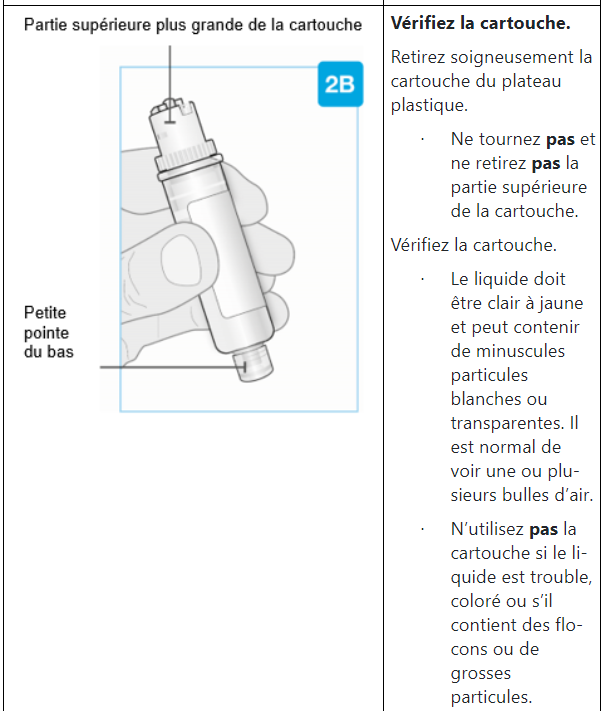
– Ne pas utiliser si le liquide visible par la fenêtre de visualisation est trouble ou contient des flocons ou de grosses particules. Le liquide doit être clair à jaune et peut contenir de minuscules particules blanches ou transparentes.
– Ne pas secouer l’emballage, la cartouche ou le dispensateur de dose.
Rapportez le médicament à la pharmacie
– si la date d’expiration (EXP) est dépassée.
– si le liquide a déjà été congelé (même s’il a été décongelé).
– si la cartouche ou le dispensateur de dose est tombé ou est endommagé.
– si les perforations du carton sont pliées.
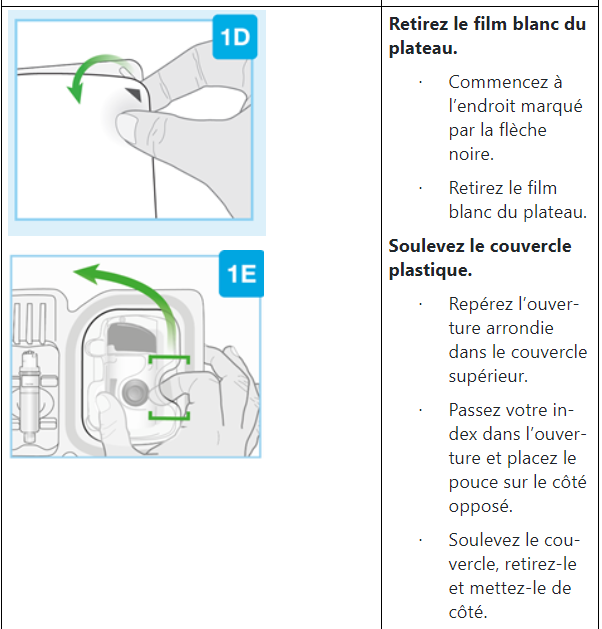
– si le couvercle blanc de la plaquette thermoformée est endommagé ou manquant.
Suivez les étapes décrites ci-dessous à chaque fois que vous utilisez SKYRIZI.
















Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 14.02.2024, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


