STELARA® solution injectable en seringue préremplie
Information destinée aux patients en Suisse
Qu’est-ce que STELARA et quand doit-il être utilisé ?
STELARA contient le principe actif «ustekinumab», un anticorps monoclonal humain. Les anticorps monoclonaux sont des protéines capables de reconnaître certaines protéines de l’organisme et de s’y fixer. STELARA bloque l’action de deux protéines de votre organisme, appelées interleukine 12 (IL-12) et interleukine 23 (IL-23). Ces protéines sont impliquées dans des processus inflammatoires du corps.
STELARA est utilisé selon prescription du médecin:
– pour le traitement du psoriasis en plaques modéré à sévère chez les adultes, chez les adolescents et les enfants à partir de 6 ans n’ayant pas répondu à d’autres médicaments ni à la photothérapie ou en cas de contre-indication ou d’intolérance à ces derniers,
– pour le traitement du rhumatisme psoriasique, seul ou en association avec le méthotrexate, chez les adultes n’ayant pas suffisamment répondu à un traitement antérieur,
– et pour le traitement de la maladie de Crohn modérée à sévère active ou de la colite ulcéreuse modérée à sévère active chez les adultes n’ayant pas suffisamment répondu à d’autres médicaments ou en cas de perte de réponse, de contre-indication ou d’intolérance à ces derniers.
Qu’est-ce que le psoriasis en plaques ?
Le psoriasis de type psoriasis en plaques est une maladie inflammatoire de la peau et des ongles. STELARA est utilisé pour atténuer les symptômes et les signes inflammatoires de votre maladie.
Qu’est-ce que le rhumatisme psoriasique (arthrite psoriasique) ?
Le rhumatisme psoriasique est une maladie inflammatoire des articulations, associée d’une manière générale au psoriasis. STELARA est utilisé pour atténuer les symptômes et les signes de votre maladie et pour améliorer vos capacités fonctionnelles physiques.
Qu’est-ce que la maladie de Crohn ou la colite ulcéreuse ?
La maladie de Crohn ou la colite ulcéreuse sont des maladies inflammatoires intestinales. STELARA est utilisé pour réduire les signes et les symptômes de la maladie.
Quand STELARA ne doit-il pas être utilisé ?
STELARA ne doit pas être utilisé si vous ou votre enfant êtes hypersensible (allergique) à l’ustekinumab ou à une autre substance contenue dans STELARA. Vous trouverez une liste complète de tous les principes actifs et de tous les excipients contenus dans STELARA au chapitre intitulé «Que contient STELARA ?».
STELARA ne doit pas non plus être utilisé si vous ou votre enfant avez une infection grave telle que p.ex. une tuberculose (voir «Quelles sont les précautions à observer lors de l’utilisation de STELARA ?»).
Quelles sont les précautions à observer lors de l’utilisation de STELARA ?
Veuillez informer votre médecin avant le traitement de toutes les maladies dont vous ou votre enfant souffrez, y compris dans les cas suivants:
– si vous ou votre enfant êtes atteint d’infections, même si elles sont très légères.
– si vous avez une plaie ouverte.
– si vous ou votre enfant avez été traité précédemment pour une tuberculose (TB) ou si vous ou votre enfant avez été récemment en contact étroit avec une personne éventuellement atteinte de la tuberculose. Le médecin vous examinera ou examinera votre enfant pour rechercher la présence éventuelle d’une tuberculose et effectuera un test permettant le cas échéant d’en prouver l’existence.
– si vous ou votre enfant souffrez actuellement d’un cancer ou si vous ou votre enfant avez été traité précédemment pour une affection cancéreuse. STELARA appartient à la famille des médicaments affaiblissant l’activité du système immunitaire (défenses immunitaires) et donc susceptibles d’augmenter le risque de cancer.
– si vous ou votre enfant avez été vacciné récemment ou si une vaccination est prévue prochainement. Informez aussi le médecin si une personne vivant dans votre ménage a besoin d’une vaccination. Les virus contenus dans certains vaccins peuvent se transmettre à des personnes dont le système immunitaire est affaibli et provoquer de graves problèmes de santé.
– si vous ou votre enfant recevez ou allez recevoir un immunosuppresseur (un médicament inhibant l’action de votre système immunitaire) ou si vous ou votre enfant êtes ou allez être sous photothérapie (un traitement consistant à exposer votre corps à un rayonnement UV spécial). STELARA agit sur le système immunitaire et l’association avec l’une de ces formes de traitement pourrait accroître le risque de maladies dues à un affaiblissement du système immunitaire, même si l’association avec ces formes de traitement n’a pas encore été étudiée.
– si vous ou votre enfant recevez ou avez reçu par le passé des injections pour traiter des allergies, en particulier des réactions allergiques graves.
– si vous ou votre enfant êtes allergique au latex.
Si vous n’êtes pas certain que l’un des points ci-dessus vous concerne ou concerne votre enfant, parlez-en à votre médecin ou à votre pharmacien avant d’utiliser STELARA.
Si vous souffrez de psoriasis, il se peut que vous présentiez un risque accru d’infarctus et d’accident vasculaire cérébral. Consultez immédiatement un médecin si vous développez des douleurs thoraciques, une faiblesse ou une sensation anormale d’un côté du corps, un affaissement du visage ou des troubles de l’élocution ou de la vision.
Informez immédiatement le médecin au cours du traitement:
– si vous constatez chez vous ou chez votre enfant des infections tenaces, ne disparaissant pas, ou des inflammations ayant une forte tendance à réapparaître. Parlez aussi à votre médecin si vous ou votre enfant présentez des signes d’infections, tels que fièvre, abattement, toux (récalcitrante), essoufflement, symptômes pseudo-grippaux ou sensations de brûlure en urinant, ou si vous ou votre enfant observez des régions de la peau chaudes, rouges ou douloureuses ou des plaies sur le corps. Ces symptômes peuvent indiquer des infections telles que des infections dans la poitrine, des infections cutanées ou encore un zona, susceptibles d’entraîner de graves complications. Il est très important d’en parler à votre médecin, car STELARA peut affaiblir les défenses immunitaires assurant la lutte contre les infections et provoquer ainsi des infections survenant principalement chez les personnes dont le système immunitaire est affaibli (infections opportunistes). Des infections opportunistes du cerveau (encéphalite, méningite), des poumons et de l’œil ont été signalées chez des patients ayant reçu un traitement par ustekinumab. Certaines inflammations pourraient considérablement s’aggraver et peut-être nécessiter un traitement hospitalier.
– si vous ou votre enfant constatez la présence de plaies ouvertes d’apparition nouvelle ou changeantes, soit au sein d’une plaque de psoriasis, soit sur la peau saine.
– si vous ou votre enfant présentez une éruption cutanée rouge, en relief et squameuse, présentant parfois une bordure foncée, dans des zones de la peau exposées au soleil, ou qui est accompagnée de douleurs articulaires. Chez certains patients, des réactions de type lupus, y compris un lupus cutané ou un syndrome de type lupus, sont survenues pendant le traitement par ustekinumab.
– si vous ou votre enfant présentez des symptômes ou des signes de réaction allergique. Ces symptômes et ces signes peuvent comprendre des difficultés respiratoires ou à avaler, une tension artérielle basse susceptible de provoquer des vertiges ou une somnolence, une éruption cutanée, un gonflement du visage, des lèvres, de la bouche ou de la gorge.
– si vous ou votre enfant souffrez de maux de tête, de convulsions ou de désorientation.
Certains types de vaccins (vaccins vivants) ne doivent pas être utilisés pendant le traitement par STELARA. Si vous avez reçu STELARA pendant la grossesse, informez le médecin de votre bébé de votre traitement par STELARA avant que le bébé ne reçoive un vaccin quelconque, y compris des vaccins vivants tels que le vaccin BCG (destiné à prévenir la tuberculose), le vaccin contre les rotavirus (destiné à empêcher les maladies gastro-intestinales provoquées par les rotavirus) ou d’autres vaccins vivants. Une exposition excessive au soleil doit être évitée et on appliquera les méthodes habituelles de protection contre les rayons solaires avec notamment l’application d’une crème solaire.
On ne sait actuellement pas si STELARA affecte l’aptitude à la conduite de véhicules et la capacité à utiliser des outils ou des machines.
Veuillez informer votre médecin ou votre pharmacien si vous ou votre enfant souffrez d’une autre maladie, si vous ou votre enfant êtes allergique ou si vous ou votre enfant prenez déjà d’autres médicaments en usage interne ou externe (même en automédication!).
STELARA peut-il être utilisé pendant la grossesse ou l’allaitement ?
Si vous êtes enceinte ou si vous envisagez une grossesse, veuillez en informer votre médecin avant le traitement. On ignore si STELARA peut affecter la fertilité.
Si vous êtes une femme en âge de procréer, il vous est conseillé de prévenir une grossesse par l’utilisation de méthodes contraceptives fiables pendant le traitement par STELARA et pendant au moins 15 semaines après la fin de ce traitement. Si vous êtes enceinte, votre médecin décidera si le bénéfice de l’utilisation de STELARA l’emporte clairement sur les risques potentiels.
L’ustekinumab peut passer dans le lait maternel en très faible quantité. Consultez votre médecin si vous allaitez ou si vous avez l’intention d’allaiter. Vous et votre médecin devez décider si vous devez plutôt interrompre STELARA pendant que vous allaitez ou si vous devez poursuivre le traitement de STELARA et ne pas allaiter.
Comment utiliser STELARA ?
Dans le traitement du psoriasis en plaques et du rhumatisme psoriasique, STELARA est injecté sous la peau («sous-cutané»).
Dans le traitement de la maladie de Crohn ou de la colite ulcéreuse, la première dose de STELARA est administrée par le personnel médical sous la forme d’une perfusion intraveineuse, puis les doses suivantes sont données par injections sous-cutanées.
Le traitement par STELARA doit être administré selon les directives et sous la surveillance de votre médecin.
Le médecin peut cependant décider de vous laisser faire les injections de STELARA vous-même. Vous recevrez dans ce cas une formation quant à la technique d’injection de STELARA. Si vous avez des questions au sujet des auto-injections ou si vous avez des doutes, adressez-vous à votre médecin. Si vous effectuez les injections sous-cutanées de STELARA vous-même, administrez STELARA en vous conformant toujours scrupuleusement aux instructions de votre médecin. Vous trouverez des informations complètes sur la technique d’injection dans le chapitre «Instructions pour l’injection sous-cutanée (sous la peau) de STELARA» à la fin de la présente notice d’emballage.
Chez les enfants et les adolescents, STELARA doit être administré par un membre du personnel médical.
Votre médecin décidera pendant combien de temps et à quelles doses le traitement par STELARA doit être administré à vous ou à votre enfant.
Demandez conseil à votre médecin en cas de doute. Convenez avec votre médecin des jours d’injections et des rendez-vous de contrôle.
Psoriasis en plaques (adultes ainsi qu’adolescents et enfants à partir de 6 ans dont le poids corporel dépasse 60 kg)
La dose habituellement recommandée est de 45 mg en injection sous-cutanée, suivie d’une nouvelle dose de 45 mg 4 semaines plus tard, puis toutes les 12 semaines. Chez les patients dont le poids corporel dépasse 100 kg, le médecin décidera s’il convient d’appliquer des doses plus élevées.
La seringue préremplie ne doit pas être utilisée chez les enfants et les adolescents dont le poids est inférieur à 60 kg. Votre médecin prescrira à votre enfant une dose de solution injectable de STELARA adaptée à son poids.
STELARA n’est pas recommandé chez les enfants de moins de 6 ans car son utilisation n’a pas été testée dans ce groupe de patients.
Rhumatisme psoriasique (adultes)
La dose habituellement recommandée est de 45 mg en injection sous-cutanée, suivie d’une nouvelle dose de 45 mg 4 semaines plus tard, puis toutes les 12 semaines. En cas de réponse insuffisante, votre médecin décidera s’il convient d’appliquer des doses plus élevées.
Maladie de Crohn ou colite ulcéreuse (adultes)
La première dose est donnée par perfusion intraveineuse. Une dose de 90 mg sera administrée par voie sous-cutanée 8 semaines après la première dose intraveineuse. Une dose de 90 mg sera administrée 12 semaines plus tard, puis toutes les 12 semaines. Votre médecin décidera s’il convient de réduire l’intervalle entre les injections à 8 semaines.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Si vous avez utilisé plus de STELARA que vous n’auriez dû (soit par l’injection d’une dose trop importante, soit par des injections trop fréquentes), parlez-en immédiatement à votre médecin ou votre pharmacien. Emportez toujours avec vous l’emballage original du médicament, même s’il est vide.
Si vous avez oublié une injection de STELARA, informez-en votre médecin ou votre pharmacien. N’injectez pas une double dose si vous avez oublié la dose précédente.
Quels effets secondaires STELARA peut-il provoquer ?
L’utilisation de STELARA peut provoquer les effets secondaires graves figurant ci-dessous. Consultez immédiatement votre médecin si vous observez l’apparition des effets indésirables suivants chez vous ou chez votre enfant:
– des signes de réaction allergique ou de réaction d’hypersensibilité grave, tels que des difficultés à respirer ou à avaler, une tension artérielle basse, des vertiges ou une somnolence, un gonflement du visage, des lèvres, de la bouche ou de la gorge entraînant des troubles respiratoires ou de la déglutition, une éruption cutanée, une urticaire, un gonflement des mains, des pieds ou des chevilles,
– des signes de réactions allergiques pulmonaires et d’inflammation pulmonaire tels que toux, difficultés respiratoires et fièvre,
– des signes d’infections (y compris la tuberculose), par exemple une fièvre, un abattement, une toux (récalcitrante), un essoufflement, des symptômes grippaux, des sudations nocturnes, une perte de poids, des diarrhées, des plaies, des problèmes dentaires, des troubles de la vue ou une perte de vision, des maux de tête, une raideur de la nuque, une sensibilité à la lumière, des nausées, une confusion ou une sensation de brûlure en urinant,
– une desquamation (une peau qui pèle) – de fortes rougeurs et une desquamation de la peau sur une surface relativement importante du corps peuvent être des signes de psoriasis érythrodermique ou de dermatite exfoliative (érythrodermie), autrement dit deux réactions cutanées graves.
L’utilisation de STELARA peut aussi provoquer les effets secondaires suivants:
Fréquent (concerne 1 à 10 personnes sur 100)
Infection des voies respiratoires supérieures, inflammation de la gorge, vertiges, maux de tête, douleurs dans la cavité bucco-pharyngée, sinusite, diarrhées, nausées, vomissements, démangeaisons, mal de dos, douleurs musculaires ou articulaires, épuisement, rougeurs et/ou douleurs au site d’injection.
Occasionnel (concerne 1 à 10 personnes sur 1000)
Inflammation des dents, inflammation du tissu sous-cutané se traduisant par une surface cutanée plus chaude, zona (herpes zoster), infections virales des voies aériennes supérieures, infections des voies aériennes inférieures, infections fongiques (champignons) vulvovaginales, réactions d’hypersensibilité, dépression, obstruction nasale, acné, modification du psoriasis avec rougeur et apparition nouvelle de minuscules vésicules blanchâtres à jaunâtres, parfois associées à de la fièvre (psoriasis pustuleux), desquamation (exfoliation) de la peau, réactions au site d’injection (entre autres saignement, hématome, durcissement, tuméfaction et démangeaisons), fatigue.
Rare (concerne 1 à 10 personnes sur 10’000)
Réactions graves, telles que réactions allergiques, gonflement rapide de la peau ou des muqueuses (angioœdème), inflammation vasculaire allergique (vascularite d’hypersensibilité), réaction pulmonaire allergique et inflammation pulmonaire se manifestant p.ex. par une toux, des difficultés respiratoires et de la fièvre.
Très rare (concerne moins d’une personne sur 10 000)
Lupus cutané ou syndrome de type lupus (éruption rouge, en relief et squameuse sur des parties de la peau exposées au soleil, pouvant être accompagnée de douleurs articulaires).
Si vous remarquez des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Conserver au réfrigérateur (2-8 °C). Ne pas congeler.
Conserver dans l’emballage d’origine pour protéger la solution de la lumière.
Si nécessaire, les seringues préremplies individuelles de STELARA peuvent être conservées dans l’emballage d’origine à température ambiante (jusqu’à 30 °C) pendant une période unique ne dépassant pas 30 jours. Notez la date de retrait du réfrigérateur de la seringue préremplie et la nouvelle date de péremption aux endroits prévus à cet effet sur la boîte. La nouvelle date de péremption ne doit pas dépasser la date de péremption initiale imprimée sur l’emballage. Dès lors qu’une seringue a été conservée à température ambiante, elle ne doit pas être remise au réfrigérateur. Jetez toute seringue conservée à température ambiante si elle n’a pas été utilisée dans les 30 jours.
N’utilisez pas STELARA si vous savez ou si vous supposez que le médicament a été exposé à des températures extrêmes (p.ex. congélation ou réchauffement involontaire).
Conserver hors de portée des enfants.
Remarques complémentaires
STELARA ne doit pas être agité. Une forte agitation prolongée de la solution pourrait affecter le médicament. N’utilisez pas le médicament s’il a été fortement secoué.
La solution pour injection de STELARA est incolore ou de couleur légèrement jaunâtre et peut contenir quelques petites particules protéiques transparentes ou de couleur blanche. Cet aspect est parfaitement normal pour des solutions contenant des protéines. Si la solution est trouble ou a changé de couleur ou si elle contient d’autres corps étrangers en suspension, il ne faut pas utiliser STELARA.
STELARA ne doit pas être mélangé avec d’autres solutions injectables.
La seringue préremplie est exclusivement destinée à un usage unique. Les restes de solution de STELARA doivent être jetés. Les aiguilles et les seringues ne doivent EN AUCUN CAS être réutilisées.
Ne pas jeter le médicament avec les eaux usées ou avec les déchets ménagers.
Demandez à votre pharmacien comment éliminer la seringue préremplie lorsque vous n’en avez plus besoin. Cette mesure contribue à la protection de l’environnement.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient STELARA ?
Principes actifs
STELARA contient le principe actif ustekinumab. Chaque seringue préremplie contient 45 mg (45 mg dans 0,5 ml) ou 90 mg (90 mg dans 1 ml) d’ustekinumab.
Excipients
STELARA contient les excipients suivants: saccharose, L-histidine, polysorbate 80 et eau pour injection.
Numéro d’autorisation
61267 (Swissmedic).
Où obtenez-vous STELARA ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
STELARA solution injectable en seringue préremplie 45 mg/0,5 ml.
STELARA solution injectable en seringue préremplie 90 mg/1 ml.
Titulaire de l’autorisation
Janssen-Cilag AG, Zoug, ZG.
Cette notice d’emballage a été vérifiée pour la dernière fois en juin 2024 par l’autorité de contrôle des médicaments (Swissmedic).
Instructions pour l’injection sous-cutanée (sous la peau) de STELARA (seringue préremplie)
Prenez tout d’abord connaissance de la notice d’emballage et lisez ensuite entièrement ces instructions avant de procéder à l’injection.
La figure 1 représente la seringue préremplie:
Figure 1:
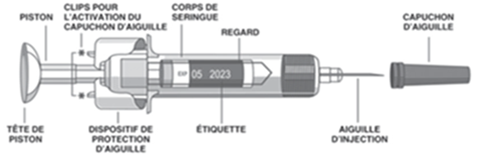
Préparation de l’injection:
1.Sortez la seringue préremplie du réfrigérateur 30 minutes avant l’utilisation, afin de l’amener à température ambiante. La seringue préremplie ne doit pas être portée à température ambiante dans de l’eau chaude. Ne retirez pas le capuchon de protection pendant la période de réchauffage!
2.Vérifiez que vous avez bien la dose prescrite, que la date d’expiration n’est pas dépassée, que l’emballage est intact et que la solution n’est pas congelée. N’utilisez pas STELARA si la solution est trouble ou a changé de couleur, ni si elle contient de gros corps étrangers en suspension.
3.Lavez-vous soigneusement les mains avec de l’eau et du savon.
4.Préparez le matériel (seringue préremplie, tampon alcoolisé, pansement).
Choix du site d’injection:
5.Choisissez l’un des trois sites d’injection (voir figure 2): face antérieure de la cuisse, ventre (mais à une distance d’au moins 5 cm du nombril) ou face externe de la partie supérieure du bras. Évitez dans toute la mesure du possible les zones cutanées atteintes par le psoriasis.
Figure 2:
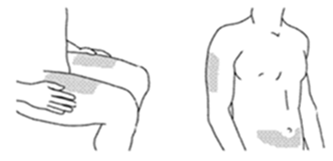
* Les zones grisées correspondent aux sites d’injection recommandés.
6.Désinfectez le site d’injection à l’aide d’un tampon imbibé d’alcool. Ne touchez plus cette zone jusqu’à l’administration de l’injection.
Injection:
7.N’utilisez pas la seringue préremplie en l’absence de capuchon de protection.
8.Retirez le capuchon de protection comme indiqué sur la figure 3.
Figure 3:

En retirant le capuchon, veillez à ne pas toucher le piston et à ne pas déformer ou faire tourner le capuchon afin d’éviter d’endommager l’aiguille.
9.Ne touchez pas l’aiguille et veillez à ce que celle-ci n’entre en contact avec aucune surface.
10.La seringue préremplie peut contenir une petite bulle visible ou présenter un peu de liquide qui perle à son extrémité. Cela est normal et n’exige aucune mesure de correction.
11.Tenez la seringue dans une main comme un stylo. De l’autre main, formez un pli de peau au niveau de la zone désinfectée.
12.Enfoncez l’aiguille d’un mouvement bref et rapide, à un angle d’environ 45° par rapport à la surface de la peau.
13.Ne tirez jamais le piston vers l’arrière!
14.Tenez maintenant le piston entre l’index et le majeur et appuyez lentement sur le piston à l’aide du pouce (voir figure 4).
Figure 4:
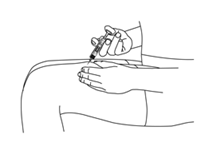
15.Enfoncez le piston complètement, jusqu’à ce que la tête de piston se trouve dans le dispositif de protection d’aiguille (voir figures 1 et 5).
Figure 5:
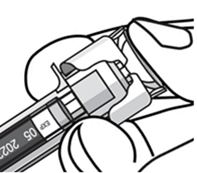
16.Maintenez la pression du pouce sur le piston lorsque vous retirez l’aiguille de la peau.
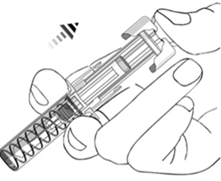
17.Le retrait de votre pouce du piston déclenche immédiatement le système de sécurité et l’aiguille est entièrement recouverte d’un capuchon de protection (voir figure 6).
Figure 6:
18.Il peut s’écouler un peu de sang ou de liquide du site d’injection. Cela est normal. Vous pouvez presser un tampon d’ouate ou une gaze sur le site d’injection et l’y maintenir durant une dizaine de secondes. Ne frottez pas le site d’injection. Si nécessaire, recouvrez le site d’injection avec un petit pansement adhésif.
Élimination de la seringue préremplie:
19.Jetez la seringue préremplie dans un récipient en verre ou en plastique pouvant être fermé hermétiquement.
20.Les tampons alcoolisés peuvent être éliminés avec les déchets ménagers.
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 17.06.2024, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans un paragraphe en gras ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 6ème mise à jour de cette page depuis le lancement début 2021 de cette rubrique. Mise à jour 1 (juin 2021). Mise à jour 2 (avril 2022). Mise à jour 3 (mars 2023). Mise à jour 4 (mai 2023). Mise à jour 5 (août 2023).
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


