Combigan®, collyre (Allergan S.A)
Information destinée aux patients en Suisse
Qu’est-ce que Combigan® et quand doit-il être utilisé ?
Combigan® est utilisé seulement selon prescription du médecin pour le traitement du glaucome à angle ouvert (glaucome).
Combigan® contient 2 substances actives différentes, la brimonidine et le timolol. Tous les deux réduisent la pression intraoculaire. La brimonidine appartient à la catégorie des substances appelées agonistes sélectifs des récepteurs α2 et le timolol aux bêtabloquants.
Votre œil contient un liquide aqueux clair, qui nourrit l’intérieur de l’œil. Ce liquide s’écoule constamment de l’œil. Pour le remplacer, l’œil produit constamment du liquide. Lorsque ce liquide ne peut pas s’évacuer de manière assez rapide, il se forme à l’intérieur de l’œil une pression qui peut altérer votre aptitude visuelle. Combigan® agit en réduisant la quantité de liquide produite dans l’œil et en augmentant la quantité de liquide évacuée. Cela entraîne une réduction de la pression intraoculaire, tandis que l’œil continue à être nourri.
De quoi faut-il tenir compte en dehors du traitement ?
Il est important de faire contrôler régulièrement la pression intraoculaire par votre médecin.
Quand Combigan® ne doit-il pas être utilisé ?
– Si vous souffrez ou avez souffert dans le passé d’une maladie respiratoire telle que l’asthme ou la bronchite obstructive chronique sévère (maladie pulmonaire grave pouvant entraîner des bruits respiratoires maladifs, des troubles respiratoires et/ou une toux chronique).
– Si vous avez des problèmes cardiaques, tels qu’une fréquence cardiaque basse, une insuffisance cardiaque, des troubles du rythme cardiaque (sauf si contrôlés par un stimulateur cardiaque).
– Si le patient est âgé de moins de 2 ans.
– Si vous prenez des médicaments tels que les inhibiteurs de la monoamine-oxydase (« inhibiteurs MAO ») ou d’autres médicaments pour le traitement de la dépression.
– Si vous êtes allergique à l’un des principes actifs ou des excipients contenus dans Combigan®.
Si vous pensez que l’un de ces points vous concerne, vous ne devez pas utiliser Combigan®, avant d’en avoir à nouveau parlé avec votre médecin.
Quelles sont les précautions à observer lors de l’utilisation de Combigan ?
Avant d’utiliser ce médicament, veuillez informer votre médecin si vous avez ou si vous avez eu dans le passé
– des problèmes psychiques
– des problèmes cardiaques ou de pression artérielle
– une diminution ou un changement de l’apport sanguin dans le cerveau, les jambes ou les bras (p. ex. maladie de Raynaud)
– du diabète ou un taux de sucre sanguin bas (hypoglycémie)
– une hyperthyroïdie
– des problèmes au niveau des reins ou du foie
– des maladies de la cornée.
Si vous avez besoin d’une anesthésie générale, informez votre médecin ou votre dentiste que vous utilisez Combigan®.
Avis aux porteurs des lentilles de contact
Le chlorure de benzalkonium peut être absorbé par les lentilles de contact souples et changer leur couleur. Retirer les lentilles de contact avant application et attendre au moins 15 minutes avant de les remettre.
Le chlorure de benzalkonium peut également provoquer une irritation des yeux, surtout si vous souffrez du syndrome de l’œil sec ou de troubles de la cornée (couche transparente à l’avant de l’œil). En cas de sensation anormale, de picotements ou de douleur dans les yeux après avoir utilisé ce médicament, contactez votre médecin.
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie,
– vous êtes allergique ou
– vous prenez déjà d’autres médicaments ou utilisez déjà d’autres médicaments à usage ophtalmique (même en automédication !).
Ceci concerne en particulier les médicaments contre l’hypertension, les médicaments pour le cœur (les glucosides cardiotoniques), les tranquillisants ou les somnifères, étant donné que leurs effets peuvent être influencés par l’utilisation concomitante de Combigan®.
Prudence s’impose lors de l’administration de Combigan® chez un enfant âgé de 2 à 17 ans parce que l’utilisation de Combigan® n’est pas recommandée chez les enfants et les adolescents.
Combigan® peut provoquer une somnolence, de la fatigue, une vision floue ou des troubles de la vision. Ces effets peuvent être accentués dans la nuit ou dans l’obscurité. Si ces effets se produisent, vous ne devez conduire aucun véhicule et ne pas utiliser de machines dangereuses. Veuillez-vous adresser à votre médecin.
Combigan® peut-il être utilisé pendant la grossesse ou l’allaitement ?
Combigan® ne doit pas être utilisé pendant la grossesse qu’avec la permission explicite de votre médecin. Veuillez informer votre médecin si vous êtes enceinte ou si vous avez l’intention de devenir enceinte.
Combigan® ne doit pas être utilisé pendant l’allaitement.
Comment utiliser Combigan® ?
Utilisez Combigan® toujours exactement selon les instructions de votre médecin. En cas de doute, veuillez-vous adresser à votre médecin ou votre pharmacien.
La posologie habituelle est : 1 goutte de Combigan® le matin et le soir dans l’œil atteint. L’intervalle de temps entre les administrations respectives doit être de 12 heures environ.
Si vous utilisez simultanément encore d’autres collyres en solution, entre l’instillation de Combigan® et l’application des autres collyres en solutions doivent être au moins 5 minutes.
Instructions pour la manipulation et l’application
N’utilisez pas le flacon si la fermeture de sécurité spéciale située sur le col du flacon est déjà endommagée, avant que vous utilisiez le collyre en solution pour la première fois.
Lavez-vous les mains avant d’ouvrir le flacon.
Inclinez la tête vers l’arrière et regardez vers le haut.
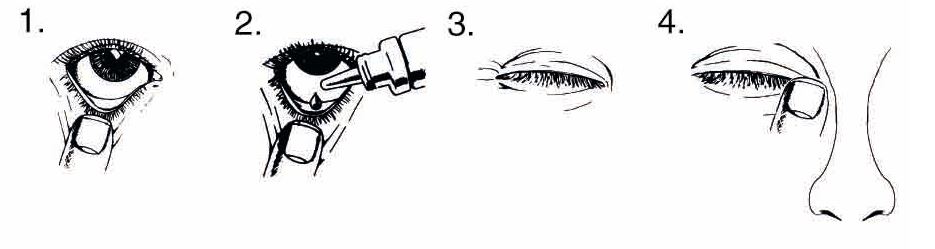
1. Tirez doucement la paupière inférieure vers le bas de manière à former une petite poche.
2. Renversez le flacon et appuyez jusqu’à ce qu’une goutte soit instillée dans l’œil à traiter.
3. Relâchez la paupière inférieure et fermez ensuite votre œil.
4. Laissez l’œil fermé et appuyez pendant une minute avec le doigt sur le coin de l’œil intérieur allant vers le nez.
Si la goutte a manqué votre œil, essayez encore une fois. Si vous administrez plus que 1 gouttes, il est improbable que cela soit nocif pour vous.
Afin d’éviter des infections éventuelles ou une lésion, l’embout du flacon ne doit pas entrer en contact avec votre œil ou avec toute autre chose. Remettez le bouchon immédiatement après utilisation pour fermer le flacon.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Surdosage
Adultes :
Si vous avez utilisé plus de Combigan® que vous n’auriez dû, il est improbable que cela soit nocif pour vous. Instillez la goutte suivante à l’heure habituelle dans l’œil. Si vous êtes incertain, adressez-vous à votre médecin ou à votre pharmacien.
Enfants :
Plusieurs cas de surdosage ont été rapportés chez des enfants lors de l’administration de brimonidine (un des principes actifs contenus de Combigan®) dans le cadre d’un traitement médicamenteux d’un glaucome. Les symptômes de surdosage de brimonidine se sont présentés tels qu’insomnie, atonie, température corporelle basse, pâleur et difficultés respiratoires.
Si ces symptômes apparaissent, contactez immédiatement votre médecin.
Adultes et enfants :
Si vous avez avalé accidentellement de Combigan®, vous devez contacter immédiatement votre médecin.
Nourrissons :
Quelques cas de surdosage ont été rapportés chez des nourrissons (jusqu’à 4 semaines), qui avaient pris de la brimonidine (un des principes actifs contenus dans Combigan®). Les signes étaient les suivants : somnolence, atonie, température corporelle basse et difficultés respiratoires. Si un de ces effets devait apparaître, contactez immédiatement votre médecin.
Application oubliée
Si vous avez oublié une application de Combigan®, rattrapez votre oubli dès que vous vous en rendez compte. Prenez la dose suivante à l’heure habituelle. Ne doublez pas votre dose pour rattraper des applications oubliées.
Quels effets secondaires Combigan® peut-il provoquer ?
Lors de l’utilisation de Combigan® les effets secondaires suivants peuvent se produire :
Effets secondaires affectant les yeux :
Très fréquents (concerne plus d’un utilisateur sur 10) : œil rouge, brûlures.
Fréquents (concerne 1 à 10 utilisateurs sur 100) : picotements ou douleurs dans l’œil, démangeaisons de l’œil ou de la paupière, réactions allergiques dans l’œil ou sur la peau entourant l’œil (des symptômes tels que œil rouge, paupière rouge ou gonflée, brûlures et picotements ou démangeaisons), gonflement, rougeur ou inflammation de la paupière, irritation ou sensation de corps étranger, follicules ou taches blanches sur la conjonctive qui recouvre la surface de l’œil, petites lésions de la surface de l’œil avec ou sans inflammation, troubles de la vision, yeux larmoyants, sécheresse oculaire, yeux collés.
Occasionnels (concerne 1 à 10 utilisateurs sur 1000) : difficultés à voir clairement, gonflement ou inflammation de la conjonctive qui recouvre la surface de l’œil, yeux fatigués, sensibilité à la lumière, douleurs de la paupière, blanchiment de la conjonctive qui recouvre la surface de l’œil, gonflement ou inflammation sous la surface de l’œil, stries dans l’œil.
Fréquence inconnue : vision floue.
Lors de l’utilisation de Combigan®, de petites quantités peuvent parvenir dans la circulation sanguine et provoquer des effets secondaires à d’autres endroits du corps.
Effets secondaires affectant le corps entier :
Fréquents (concerne 1 à 10 utilisateurs sur 100) : dépression, somnolence, maux de tête, hypertension, sécheresse buccale, faiblesse générale.
Occasionnels (concerne 1 à 10 utilisateurs sur 1000) : torpeur, insuffisance cardiaque, perte de connaissance, sécheresse nasale, fréquence cardiaque irrégulière, modification de la perception gustative, nausée, diarrhée.
Fréquence inconnue : augmentation ou diminution de la fréquence cardiaque, tension artérielle basse, rougeur de la face.
Les effets secondaires suivants se sont produits avec la brimonidine seul et peuvent donc apparaître éventuellement avec Combigan®: inflammation dans l’œil, pupilles petites, troubles du sommeil (insomnie), symptômes analogues au rhume, essoufflement, troubles gastriques, aigreurs d’estomac, troubles du comportement alimentaire, réactions allergiques générales, réactions cutanées incluant éruption cutanée, peau rougie ou démangeaison, gonflement de la face, démangeaison sur tout le corps et dilatation des vaisseaux sanguins.
Comme d’autres médicaments administrés à l’œil, Combigan® est absorbé dans le sang. L’absorption du timolol, une composante bêtabloquante contenu dans Combigan® peut provoquer des effets secondaires similaires à ceux observés avec les bêtabloquants « intraveineux » et/ou « oraux ». La fréquence des effets secondaires après une application locale est plus faible qu’après une application orale ou intraveineuse, par exemple. Les effets secondaires mentionnés comprennent les réactions observées avec la classe des bêtabloquants utilisés dans le traitement des maladies oculaires :
– réactions allergiques généralisées incluant gonflements sous la peau (pouvant se produire au niveau du visage ou des membres et pouvant obstruer les routes aériennes résultant dans des difficultés à avaler ou à respirer), urticaire (ou éruption cutanée qui démange), éruption cutanée localisée ou généralisée, démangeaisons, réactions allergiques sévères soudaines à danger de mort
– taux de glycémie bas
– troubles de sommeil, cauchemars, hallucinations, anxiété, perte de mémoire, confusion
– accident vasculaire cérébral, diminution du flux sanguin vers le cerveau, augmentation des signes et symptômes de la myasthénie grave (maladie musculaire), perceptions sensorielle anormale (tel que des piqûres d’épingles, picotement, engourdissement)
– inflammation de la cornée, détachement de la rétine (détachement de la couche en dessous de la rétine – qui contient des vaisseaux sanguins – après une opération destinée à réduire la pression dans l’œil pouvant causer des troubles visuels), œdème maculaire cystoïde (gonflement dans l’intérieur de la rétine qui est la couche sensible à la lumière de l’œil), diminution de la sensibilité de la cornée, affaissement de la paupière (fermant l’œil à moitié), vision double
– bourdonnement dans les oreilles (acouphènes)
– aggravation des douleurs thoraciques, œdèmes (accumulation de liquide), une forme de trouble du rythme cardiaque, attaque cardiaque, arrêt du cœur, faiblesse du myocarde
– mal aux jambes (claudication), les doigts des mains et pieds devient blancs (Phénomène de Raynaud), des mains et des pieds froids
– rétrécissement des voies respiratoires dans les poumons (particulièrement chez les patients présentant des maladies des voies respiratoires), difficultés à respirer, toux, défaillance respiratoire
– troubles de la digestion, douleurs abdominales, vomissements
– perte de cheveux, éruption cutanée de couleur blanche-argentée (rash psoriasiforme) ou aggravation d’un psoriasis
– douleur musculaire non causé par l’exercice physique
– déformation du pénis (maladie de Peyronie), dysfonctionnements sexuels, baisse de la libido
– fatigue.
Ce médicament contient 25,8 mg de phosphates par 1 ml.
Si vous souffrez de dommages sévères de la cornée (couche transparente située à l’avant de l’œil) les phosphates peuvent causer, dans de très rares cas, des troubles de la vision en raison de l’accumulation de calcium pendant le traitement (nuage).
Si vous remarquez toutefois des effets secondaires, veuillez en informer votre médecin ou votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention « Exp » sur le récipient.
Délai d’utilisation après ouverture
À utiliser dans les 4 semaines après ouverture. Cela aide à éviter des infections. Notez la date de la première ouverture dans l’espace réservé à cet effet sur le carton, afin de vous en souvenir plus facilement.
Remarques concernant le stockage
Conservez à température ambiante (15–25°C). Conserver le récipient dans son carton pour le protéger de la lumière.
Tenir hors de la portée des enfants.
Après la fin du traitement, ou au plus tard 4 semaines après la première ouverture du flacon, veuillez rapporter le médicament avec le contenu restant à la personne qui vous l’a délivré (médecin ou pharmacien) en vue de son élimination conforme.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Combigan® ?
1 ml de Combigan® contient :
Principes actifs : 2 mg de tartrate de brimonidine et 5 mg de timolol.
Excipients : chlorure de benzalkonium, phosphate de sodium monobasique monohydraté, phosphate de sodium dibasique heptahydraté, eau purifiée. De petites quantités d’acide chlorhydrique ou d’hydroxyde de sodium peuvent être ajoutées pour amener la solution au bon pH (mesure de l’acidité ou de l’alcalinité de la solution).
Numéro d’autorisation
56947 (Swissmedic)
Où obtenez-vous Combigan® ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Les emballages suivants sont disponibles :
Emballage avec 1 flacon contenant 5 ml de Combigan® collyre en solution.
Emballage avec 3 flacons contenant chacun 5 ml de Combigan® collyre en solution.
Titulaire de l’autorisation
Allergan S.A., Cham
Cette notice d’emballage a été vérifiée pour la dernière fois en juin 2019 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 01.09.2021, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


