Vistagan® Liquifilm® 0,5% Unit Dose, collyre (Allergan S.A)
Information destinée aux patients en Suisse
Qu’est-ce que VISTAGAN® LIQUIFILM® 0,5% Unit Dose et quand doit-il être utilisé ?
VISTAGAN® LIQUIFILM® 0,5% Unit Dose est un collyre sans conservateur délivré uniquement selon prescription du médecin pour le traitement d’une pression intraoculaire élevée et du glaucome chronique à angle ouvert. VISTAGAN® LIQUIFILM® 0,5% Unit Dose ne contient pas d’agents conservateurs. C’est pourquoi il peut être utilisé à la suite d’opérations des yeux ou lorsque vous réagissez avec une hypersensibilité aux agents conservateurs.
Votre œil contient un liquide aqueux qui s’écoule constamment de l’œil et qui est remplacé par du liquide nouvellement formé. Lorsque ce liquide ne peut pas s’évacuer de manière assez rapide, un glaucome peut se développer et la pression peut augmenter à l’intérieur de l’œil et finalement altérer votre vision. VISTAGAN® LIQUIFILM® 0,5% Unit Dose agit en réduisant la quantité de liquide produite dans l’œil. Cela entraîne une réduction de la pression intraoculaire.
VISTAGAN® LIQUIFILM® 0,5% Unit Dose fait partie du groupe de médicaments appelés bêtabloquants.
De quoi faut-il tenir compte en dehors du traitement ?
Ce médicament vous a été prescrit par votre médecin dans le but de traiter les troubles oculaires dont vous souffrez actuellement. Ne l’utilisez pas de votre propre initiative pour le traitement d’autres maladies ou chez d’autres personnes.
Avis aux porteurs de lentilles de contact
Les lentilles de contact doivent être retirées avant chaque utilisation de VISTAGAN® LIQUIFILM® 0,5% Unit Dose, puis n’être remises en place qu’au bout de 15 minutes.
Quand VISTAGAN® LIQUIFILM® 0,5% Unit Dose ne doit-il pas être utilisé ?
VISTAGAN® LIQUIFILM® 0,5% ne doit pas être utilisé:
– Si vous présentez une hypersensibilité connue ou suspectée (allergie) à l’un des composants de VISTAGAN® LIQUIFILM® 0,5% Unit Dose.
– Si vous souffrez ou avez par le passé souffert d’asthme ou d’autres affections pulmonaires chroniques avec troubles respiratoires, essoufflement, sifflements respiratoires ou toux chronique.
– Si vous souffrez ou avez par le passé souffert de problèmes cardiaques tels qu’un rythme cardiaque lent, des troubles du rythme cardiaque (dans la mesure où ils ne sont pas contrôlés par un pacemaker) ou de maladies cardiaques sévères (insuffisance cardiaque).
L’utilisation de VISTAGAN® LIQUIFILM® 0,5% Unit Dose est déconseillé chez l’enfant et l’adolescent.
Quelles sont les précautions à observer lors de l’utilisation de VISTAGAN® LIQUIFILM® 0,5% Unit Dose ?
Avant d’appliquer VISTAGAN® LIQUIFILM® 0,5% Unit Dose, veuillez parler à votre médecin ou à votre pharmacien si vous souffrez ou avez par le passé souffert de l’une des maladies suivantes:
– Asthme ou problèmes respiratoires
– Problèmes cardiaques (y compris insuffisance cardiaque, troubles du rythme cardiaque et rythme cardiaque lent)
– Problèmes de tension artérielle (chute de la tension artérielle après s’être mis en position debout)
– Douleurs thoraciques au repos (angor de Prinzmetal)
– Mauvaise circulation sanguine, en particulier dans le cerveau, les jambes, les bras et les mains
– Diabète ou diminution soudaine du taux de sucre dans le sang (hypoglycémie)
– Troubles de la thyroïde
– Toutes allergies (en particulier lorsqu’elles sont sévères)
– Inflammations oculaires chroniques ou en cas de problèmes de cornée
– Opérations des yeux pour faire baisser la pression intraoculaire.
Si vous avez, par le passé, présenté des troubles respiratoires ou des affections cardiaques, il se peut que votre médecin vous surveille plus étroitement, car de rares cas de décès ont été rapportés après utilisation de lévobunolol.
Si vous souffrez d’allergies ou que vous faites une réaction allergique sévère, il se peut que, le cas échéant, la dose habituelle d’adrénaline doive être augmentée.
Veuillez immédiatement informer votre médecin si vous présentez une irritation oculaire ou si de nouveaux problèmes oculaires surviennent (y compris rougeurs ou démangeaisons oculaires).
Si vous avez besoin d’une anesthésie générale, veuillez informer votre médecin ou votre dentiste que vous êtes traités par VISTAGAN® LIQUIFILM® 0,5% Unit Dose.
Informez votre médecin ou votre pharmacien si vous prenez d’autres bêtabloquants.
Étant donné que VISTAGAN® LIQUIFILM® 0,5% Unit Dose est également un bêtabloquant, votre médecin doit être informé s’il existe éventuellement un risque que votre organisme reçoive trop de bêtabloquants. Les symptômes suivants peuvent indiquer la présence d’un tel risque:
– Tension artérielle basse (p.ex. en se relevant)
– Rythme cardiaque lent
– Vertiges/perte de conscience passagère
– Faible pression intraoculaire.
L’aptitude à conduire un véhicule ou à utiliser des machines peut être altérée en raison de possibles effets secondaires de VISTAGAN® LIQUIFILM® 0,5% Unit Dose comme p.ex. fatigue, vertiges ou vision floue/altérée. Ne conduisez pas et n’utilisez pas de machine jusqu’à ce que ces symptômes disparaissent.
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie,
– vous êtes allergique ou
– vous prenez déjà d’autres médicaments (même en automédication) ou utilisez d’autres médicaments à usage ophtalmique!
Ceci s’applique en particulier aux médicaments suivants:
– Médicaments pour le traitement de la tension artérielle élevée (hypertension)
– Médicaments pour le traitement de maladies cardiaques (p.ex. battements cardiaques irréguliers), tels que des bêtabloquants, de l’amiodarone ou de la digoxine
– Autres collyres pour faire baisser la pression intraoculaire élevée (glaucome)
– Médicaments pour dilater les pupilles, p.ex. adrénaline
– Médicaments pour le traitement du diabète ou des taux élevés de sucre dans le sang
– Autres bêtabloquants pris par voie orale ou utilisés comme collyres.
VISTAGAN® LIQUIFILM® 0,5% Unit Dose peut-il être utilisé pendant la grossesse ou l’allaitement ?
Si vous êtes enceinte ou envisagez une grossesse, vous ne devez pas utiliser VISTAGAN® LIQUIFILM® 0,5% Unit Dose que sur prescription formelle de votre médecin ou de votre pharmacien.
De même, vous ne devez pas utiliser VISTAGAN® LIQUIFILM® 0,5% Unit Dose pendant l’allaitement que sur prescription formelle de votre médecin ou votre pharmacien.
Comment utiliser VISTAGAN® LIQUIFILM® 0,5% Unit Dose ?
Adultes:
Sauf prescription contraire du médecin, débuter le traitement en instillant 1 goutte de VISTAGAN® LIQUIFILM® 0,5% Unit Dose dans le sac conjonctival de l’œil atteint 2x/jour (matin et soir). Si la pression intraoculaire se stabilise, le médecin traitant peut envisager une application 1x/jour. Veuillez suivre scrupuleusement les recommandations de votre médecin!
L‘utilisation et la sécurité de VISTAGAN® LIQUIFILM® 0,5% Unit Dose n‘ont pas été étudiées chez l‘enfant et l‘adolescent.
Votre médecin contrôlera en général votre pression intraoculaire quatre semaines après le début de traitement. Il peut éventuellement être nécessaire d’utiliser un autre médicament en plus de VISTAGAN® LIQUIFILM® 0,5% pour ajuster votre pression intraoculaire.
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Instructions concernant l’application
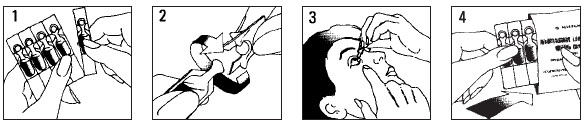
1. Lavez-vous les mains. Ouvrez l’un des sachets en aluminium contenant chacun deux bandes de cinq récipients unidoses. Avant de l’utiliser, assurez-vous que le récipient unidose n’est pas endommagé. Le collyre doit être utilisé immédiatement après ouverture. Détachez un des récipients unidose de la bande.
2. Tenez le récipient unidose à la verticale (avec le bouchon vers le haut) et détachez le bouchon en tournant.
3. Penchez la tête en arrière et regardez le plafond. Tirez doucement la paupière inférieure vers le bas afin de manière à former une petite poche, puis pressez sur le récipient à ce qu’une goutte soit instillée dans chaque œil à traiter. Fermez l’œil traité et pressez le bout du doigt sur le coin intérieur de l’œil (le coin allant vers le nez) pendant 2 minutes.
4. Remettez les récipients unidoses dans le sachet en aluminium et conservez-les dans la boîte.
Répétez les étapes 3 et 4 pour l’autre œil s’il doit également être traité.
Répétez la procédure si la goutte n’est pas tombée dans votre œil.
Afin d’éviter une contamination, l’ouverture du récipient unidose ne doit pas entrer pas en contact avec l’œil ou quoi que ce soit d’autre.
Les récipients unidoses sont destinés à un usage unique. C’est pourquoi, même s’il reste encore un peu de solution, celle-ci ne doit pas être conservée en vue d’une utilisation ultérieure.
Essuyez tout excès de liquide présent sur votre joue avec un linge propre.
Il est très important d’utiliser correctement le collyre. Si vous avez des questions, adressez-vous à votre médecin ou à votre pharmacien.
Si vous avez instillé plus de VISTAGAN® LIQUIFILM® 0,5% Unit Dose que vous devriez, il est improbable que des effets secondaires surviennent. Si vous avez instillé trop de gouttes dans votre œil/vos yeux, lavez-le/les à l’eau claire. Appliquez la prochaine dose à l’heure habituelle.
Si le médicament a été bu accidentellement, contactez immédiatement votre médecin ou votre pharmacien.
Si vous avez oublié d’appliquer une dose de VISTAGAN® LIQUIFILM® 0,5% Unit Dose, vous devez la rattraper dès que vous y pensez, à moins qu’il ne soit presque l’heure de l’instillation suivante. Dans ce cas, n’instillez pas la dose oubliée. Reprenez ensuite l’instillation suivante à l’heure habituelle. N’instillez pas de dose double pour compenser la dose que vous avez oubliée.
N’arrêtez pas ou ne diminuez pas l’application de VISTAGAN® LIQUIFILM® 0,5% Unit Dose avant que votre médecin vous y invite, car vos symptômes pourraient alors s’aggraver.
VISTAGAN® LIQUIFILM® 0,5% Unit Dose doit être utilisé selon les instructions de votre médecin. Si vous avez d’autres questions, adressez-vous à votre médecin ou à votre pharmacien.
Quels effets secondaires VISTAGAN® LIQUIFILM® 0,5% Unit Dose peut-il provoquer ?
Les effets indésirables suivants peuvent survenir lors de l’utilisation de VISTAGAN® LIQUIFILM® 0,5% Unit Dose:
Les principes actifs contenus dans les collyres peuvent entrer dans la circulation sanguine. C’est pourquoi on peut aussi observer la survenue d’effets indésirables dans d’autres parties du corps que l’œil.
Très fréquents (chez plus de 10 patients sur 100): irritation oculaire, douleurs oculaires.
Fréquents (chez 1-10 patients sur 100): inflammation de la conjonctive (couche transparente qui recouvre la surface de l’œil) et de la paupière.
Occasionnels (chez 1-10 patients sur 1000): rythme cardiaque lent, tension artérielle basse.
Rares: inflammation de l’iris, maux de tête, urticaire, démangeaison, faiblesse, fatigue.
Fréquence non connue: rougeur de l’œil, inflammation allergique de la conjonctive (couche transparente qui recouvre la surface de l’œil), baisse de la sensibilité de la surface de votre œil, inflammation dans l’œil ou à la surface de l’œil, vision floue, démangeaisons dans les yeux/sur les paupières, gonflement de l’œil/de la paupière, écoulements oculaires ou larmes, sécheresse oculaire, petites déchirures à la surface de l’œil avec ou sans inflammation, rougeur de la paupière, eczéma sur la paupière, inflammation cutanée sur la paupière, sensation de corps étranger dans l’œil, dépression, confusion, vertiges, somnolence, baisse d’énergie, troubles du sommeil, évanouissement, pause cardiaque, rythme cardiaque irrégulier ou rapide, mains, pieds et extrémités gonflés ou froids dus à la constriction de vos vaisseaux sanguins, asthme, difficultés respiratoires, gorge irritée, problèmes de nez, nausées, éruption cutanée, peau qui pèle et qui démange, zones de peau rêches, rougeur de la peau, gonflement du visage, chute des cheveux, symptômes d’une réaction allergique (gonflement, rougeur de l’œil et éruptions cutanés.
Les effets indésirables suivants peuvent survenir avec d’autres collyres du groupe des bêtabloquants; ils peuvent par conséquent aussi survenir avec VISTAGAN® LIQUIFILM® 0,5% Unit Dose, étant donné qu’il fait également partie de ce groupe:
Fréquence non connue: séparation de l’une des couches dans le globe oculaire après une intervention chirurgicale pour réduire la pression à l’intérieur de l’œil, troubles visuels, vision double, paupière tombante, réactions allergiques graves avec gonflement et difficultés respiratoires, douleurs thoraciques, rythme cardiaque irrégulier, défaillance cardiaque, trop d’accumulation de liquide dans l’organisme, essentiellement de l’eau, sifflements respiratoires, toux, flux sanguin réduit dans le cerveau, accident vasculaire cérébral (AVC), perte de mémoire, cauchemars, faiblesse musculaire accrue (aggravation d’une myasthénie grave), fourmillements, faible taux de sucre dans le sang, douleurs abdominales, vomissements, diarrhée, troubles digestifs, bouche sèche, modifications de votre sensibilité gustative, taches rouges squameuses sur la peau, douleurs musculaires, diminution de la libido, troubles sexuels.
Patients souffrants d’une maladie pulmonaire, d’une maladie cardiaque ou cardiovasculaire, et des troubles qui y correspondent doivent en prévenir le médecin avant d’utiliser VISTAGAN® LIQUIFILM® 0,5% Unit Dose.
Dès que l’un des effets indésirables suivants survient, vous devez immédiatement consulter votre médecin:
– Troubles respiratoires (y compris de l’asthme)
– Rythme cardiaque inhabituel ou lent
– Éruption cutanée, troubles de la déglutition, gonflement des lèvres, du visage, de la gorge ou de la langue (il pourrait s’agit de signes d’une réaction allergique grave)
– Perte de conscience (ou si vous avez une sensation correspondante)
– Tension artérielle basse
– Autres signes inhabituels.
Les effets indésirables susmentionnés sont graves et peuvent dans certains cas mettre votre vie en danger.
Vous devez immédiatement consulter votre médecin ou pharmacien en cas de survenue d’autres effets indésirables pour lesquels vous supposez qu’ils sont en rapport avec l’utilisation de VISTAGAN® LIQUIFILM® 0,5% Unit Dose.
Si vous remarquez des effets secondaires qui ne sont pas mentionnés dans cette notice, veuillez en informer votre médecin ou votre pharmacien.
À quoi faut-il encore faire attention ?
Stabilité
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «Exp» sur l’emballage.
Conservation/stockage
Tenir hors de la portée des enfants.
Conserver à température ambiante (15-25°C) et à l’abri de la lumière dans l’emballage d’origine.
Les récipients unidoses doivent toujours être conservés dans le sachet en aluminium et dans la boîte. Toute solution non utilisée doit être jetée car elle ne contient pas de conservateurs.
À la fin du traitement, veuillez rapporter le médicament avec le contenu restant à la personne qui vous l’a délivré (médecin ou pharmacien) en vue de son élimination conforme.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient VISTAGAN® LIQUIFILM® 0,5% Unit Dose ?
1 ml VISTAGAN® LIQUIFILM® 0,5% Unit Dose contient:
Principe actif: chlorhydrate de lévobunolol 5 mg.
Excipients: édétate de sodium, alcool polyvinylique, monohydrogénophosphate de sodium heptahydrate, dihydrogénophosphate de potassium, chlorure de sodium, hydroxyde de sodium ou acide chlorhydrique, eau purifiée.
Numéro d’autorisation
51798 (Swissmedic)
Où obtenez-vous VISTAGAN® LIQUIFILM® 0,5% Unit Dose ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Emballage avec 30 récipients unidoses contenant chacun 0,4 ml de collyre en solution.
Emballage avec 60 récipients unidoses contenant chacun 0,4 ml de collyre en solution.
Titulaire de l’autorisation
Allergan S.A., Cham
Cette notice d’emballage a été vérifiée pour la dernière fois en février 2019 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 01.09.2021, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


