Cypestra-35® Dragées
Information destinée aux patients en Suisse
Qu’est-ce que Cypestra-35 et quand doit-il être utilisé ?
Selon prescription du médecin.
Cypestra-35 est un médicament contenant deux hormones: l’éthinylestradiol, une hormone féminine (appelée oestrogène) et l’acétate de cyprotérone, qui inhibe d’une part l’effet des hormones masculines et possède d’autre part des propriétés d’hormone du corps jaune.
Cypestra-35 est prescrit par le médecin à des femmes souffrant de maladies dépendant des hormones masculines, telles que:
– Une acné modérée à sévère (associée ou non à une peau très grasse, c.-à-d. une séborrhée), lorsque les traitements locaux ou les traitements antibiotiques oraux n’ont pas entraîné d’amélioration,
– une pilosité excessive, pathologique, du visage et du corps (hirsutisme).
Si la forte pilosité est récente ou si elle s’est considérablement aggravée ces derniers temps, il faut le signaler expressément au médecin, une recherche diagnostique des causes étant alors nécessaire.
Bien que Cypestra-35 ait aussi un effet anticonceptionnel, il ne doit être utilisé que chez des patientes devant recevoir un traitement hormonal pour les tableaux cliniques décrits ci-dessus et ne doit pas être utilisé en même temps qu’un autre contraceptif hormonal.
Informations importantes sur Cypestra-35
– Cypestra-35 augmente légèrement le risque de formation d’un caillot sanguin dans les veines et les artères, notamment pendant la première année de prise ou lorsque la prise de Cypestra-35 est reprise après une interruption de 4 semaines ou plus.
– Soyez attentif aux symptômes d’un caillot sanguin et adressez-vous à votre médecin si vous pensez les présenter (voir «Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?», «Effets sur la coagulation sanguine, risque de maladies vasculaires»).
De quoi faut-il tenir compte en dehors du traitement ?
Avant de commencer à prendre Cypestra-35, veuillez lire les informations relatives aux caillots sanguins à la rubrique «Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?». Il est particulièrement important de lire les informations sur les symptômes d’un caillot sanguin (cf. «Comment reconnaître un caillot sanguin»).
Avant que vous ne commenciez ou recommenciez à prendre Cypestra-35, votre médecin devra s’informer avec précision de vos antécédents médicaux personnels et familiaux (maladies dont vous avez souffert ou survenues dans votre famille) et réaliser un examen général et gynécologique approfondi. L’éventualité d’une grossesse doit être exclue.
Durant la prise de Cypestra-35, il est recommandé de pratiquer des examens de contrôle réguliers en accord avec votre médecin. Il évaluera les risques que vous présentez éventuellement (comme l’âge, le poids, une intervention chirurgicale, une modification de votre état de santé et/ou de vos facteurs de risque) par rapport au bénéfice attendu et décidera avec vous de la poursuite du traitement.
Cypestra-35 a une composition similaire à celle d’une pilule contraceptive combinée, mais ne doit pas être pris uniquement comme contraceptif.
Le risque de malformations est augmenté si une grossesse survient pendant la prise de Cypestra-35. Il est donc très important de prendre régulièrement Cypestra-35 conformément aux recommandations de dosage, afin de garantir une contraception fiable.
Si vous avez pris jusqu’ici un contraceptif hormonal et que vous voulez commencer à prendre Cypestra-35, veuillez d’abord demander l’avis de votre médecin.
Les contraceptifs hormonaux pris précédemment doivent être arrêtés (cf. «Comment utiliser Cypestra-35 ?» – «Début de la prise»).
Le risque de formation de caillots sanguins est augmenté immédiatement après l’accouchement. Vous devez donc demander à votre médecin quand vous pouvez recommencer à prendre Cypestra-35.
Cypestra-35 ne protège pas des infections à VIH (SIDA) ni d’autres maladies sexuellement transmissibles.
Quand Cypestra-35 ne doit-il pas être pris ?
Cypestra-35 ne doit pas être pris si l’une des situations suivantes vous concerne.
Si l’une des situations suivantes vous concerne, vous devez en informer votre médecin. Votre médecin vous indiquera alors quel autre traitement vous convient mieux.
– Si vous avez (ou avez eu par le passé) un caillot de sang dans un vaisseau sanguin de la jambe (thrombose veineuse profonde de la jambe), du poumon (embolie pulmonaire) ou d’un autre organe;
– si vous avez déjà eu un infarctus du myocarde ou un accident vasculaire cérébral (attaque cérébrale);
– si vous avez (ou avez déjà eu) une angine de poitrine (une maladie causant de fortes douleurs dans la poitrine et pouvant être le premier signe d’un infarctus du myocarde) ou un accident ischémique transitoire (symptômes passagers d’un accident vasculaire cérébral);
– si vous savez que vous êtes atteint d’un trouble de la coagulation sanguine, par exemple déficit en protéine C, déficit en protéine S, déficit en antithrombine III, mutation du facteur V de Leiden ou présence d’anticorps anti-phospholipides;
– si l’un de vos frères et soeurs ou de vos parents a présenté un caillot de sang à un âge relativement jeune (avant l’âge de 50 ans);
– si vous présentez simultanément plusieurs facteurs de risque de survenue d’un caillot sanguin, p.ex. un surpoids ou un âge >35 ans (cf. chapitre «Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?» – «Facteurs augmentant le risque de caillot sanguin dans une veine» et «Facteurs augmentant le risque de caillot sanguin dans une artère»);
– si vous souffrez ou avez souffert par le passé d’une forme particulière de migraine (dite «migraine avec aura» qui s’accompagne de troubles de la sensibilité, de la perception et/ou des mouvements);
– si vous souffrez d’un diabète sévère (diabète sucré) avec des complications vasculaires;
– si votre pression artérielle est très élevée;
– si vos taux de graisses dans le sang (cholestérol et triglycérides) sont très élevés;
– si vous avez ou avez eu un cancer du sein ou de l’utérus, dans lequel les hormones sexuelles jouent ou jouaient un rôle (hormono-dépendance);
– si vous avez des hémorragies vaginales inexpliquées;
– si vous souffrez ou avez souffert de maladies graves du foie (p.ex. jaunisse) aussi longtemps que les paramètres de la fonction hépatique ne sont pas revenus à la normale;
– si vous avez ou avez eu des tumeurs du foie;
– si vous souffrez d’hépatite C et prenez des médicaments antiviraux qui contiennent de l’ombitasvir/du paritaprévir/du ritonavir, du dasabuvir du glécaprévir/du pibrentasvir ou du sofosbuvir/du velpatasvir/du voxilaprévir (voir également la rubrique «Interactions avec d’autres médicaments»);
– en cas de grossesse confirmée ou présumée;
– pendant l’allaitement;
– si vous utilisez en même temps un contraceptif hormonal;
– en cas d’hypersensibilité à l’un des composants de Cypestra-35.
Si l’une des situations mentionnées ci-dessus survient pour la première fois pendant la prise de Cypestra-35, consultez votre médecin et appliquez des méthodes contraceptives non hormonales.
Cypestra-35 n’est pas indiqué dans le cadre d’un traitement chez l’homme.
Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?
Vous devez consulter sans délai un médecin si vous présentez les symptômes suivants (cf. Tableau «Comment reconnaître un caillot sanguin»):
– Migraine d’apparition récente ou maux de tête intenses inhabituels;
– troubles respiratoires soudains ou apparition soudaine d’une toux sans cause évidente;
– douleurs inexpliquées au niveau des jambes avec ou sans gonflement;
– troubles visuels, auditifs, de la parole ou autres troubles sensoriels, d’apparition soudaine;
– douleur intense et soudaine dans la partie supérieure de l’abdomen ou dans la cage thoracique avec ou sans irradiation dans le bras;
– apparition soudaine de vertiges, d’une sensation de faiblesse, de troubles de la sensibilité;
– collapsus avec ou sans convulsions;
– au moins 4 semaines avant des opérations programmées et pendant la convalescence après un accident ou une opération;
– nette augmentation de la pression artérielle lors de plusieurs mesures;
– dépression;
– jaunisse;
– grossesse ou suspicion de grossesse.
Il est important que vous informiez votre médecin si vous souffrez ou avez souffert des maladies suivantes ou si celles-ci s’aggravent ou apparaissent pour la première fois pendant le traitement par Cypestra-35
– Si vous avez des règles irrégulières, certaines modifications des seins, un cancer du sein dans la famille ou une tumeur bénigne de l’utérus (myome);
– si vous avez une rétention de liquide dans les tissus (oedèmes);
– si vous avez des maladies graves des reins;
– si vous avez une épilepsie ou une danse de Saint Guy (chorée de Sydenham);
– si vous avez des dépressions;
– si vos taux de graisses dans le sang sont élevés (hypertriglycéridémie) ou si l’un des membres de votre famille a été atteint de cette pathologie. Une augmentation du risque de pancréatite (inflammation du pancréas) a été rapportée lorsque Cypestra-35 a été pris en présence d’une hypertriglycéridémie;
– si vous souffrez d’une inflammation d’une veine (thrombophlébite superficielle);
– si vous avez des varices;
– si vous avez une jaunisse ou des affections de la vésicule biliaire;
– si vous souffrez de la maladie de Crohn ou de colite ulcéreuse (rectocolite hémorragique) (maladie inflammatoire chronique de l’intestin);
– si vous souffrez d’un lupus érythémateux disséminé (LED – une maladie affectant votre système de défense naturel);
– si vous souffrez d’un syndrome hémolytique et urémique (SHU – un trouble de la coagulation sanguine entraînant une défaillance rénale);
– si vous avez une drépanocytose (une maladie rare du sang);
– si vous avez eu une maladie ressemblant à un herpès lors d’une précédente grossesse (herpes gestationis);
– si vous avez une surdité de l’oreille moyenne (otosclérose);
– si vous souffrez d’une anomalie de la production d’hémoglobine (porphyrie).
Dans de rares cas, des taches brunâtres (chloasma) peuvent apparaître sur le visage, en particulier si ce phénomène s’est manifesté lors d’une grossesse antérieure. Si vous avez une telle prédisposition, vous devez éviter les bains de soleil prolongés et les rayons ultraviolets pendant la prise de Cypestra-35.
Chez les patientes présentant un angio-oedème héréditaire ou acquis (gonflement de la peau et des muqueuses), la prise d’oestrogènes peut déclencher un angiooedème ou accentuer les symptômes.
Effets sur la coagulation sanguine, risque de maladies vasculaires
Le terme de thrombose désigne la formation d’un caillot de sang qui peut boucher un vaisseau sanguin.
Lorsque vous prenez Cypestra-35, votre risque de formation d’un caillot de sang est plus élevé que si vous ne prenez pas Cypestra-35.
Les caillots de sang peuvent survenir
– dans les veines («thrombose veineuse», «thromboembolie veineuse»)
– dans les artères («thrombose artérielle», «thromboembolie artérielle»).
Il se produit le plus souvent une thrombose dans les veines profondes des jambes (thrombose veineuse profonde). Si un caillot sanguin se détache de la paroi veineuse, il peut se déplacer et obstruer les artères pulmonaires, conduisant à ce qu’on appelle une embolie pulmonaire. Très rarement, des caillots de sang peuvent aussi apparaître dans les vaisseaux sanguins du coeur, pouvant alors déclencher un infarctus. Les caillots sanguins ou l’éclatement de vaisseaux sanguins dans le cerveau peuvent être la cause d’un accident vasculaire cérébral.
Il est très rare que des caillots de sang puissent se former dans d’autres parties du corps telles que le foie, l’intestin, les reins ou les yeux.
Les événements thromboemboliques veineux ou artériels peuvent dans de rares cas avoir des conséquences lourdes et durables sur la santé ou avoir une issue fatale.
COMMENT RECONNAÎTRE UN CAILLOT SANGUIN
Vous devez arrêter immédiatement la prise de Cypestra-35 et consulter sans délai un médecin lors de la survenue des signes suivants:
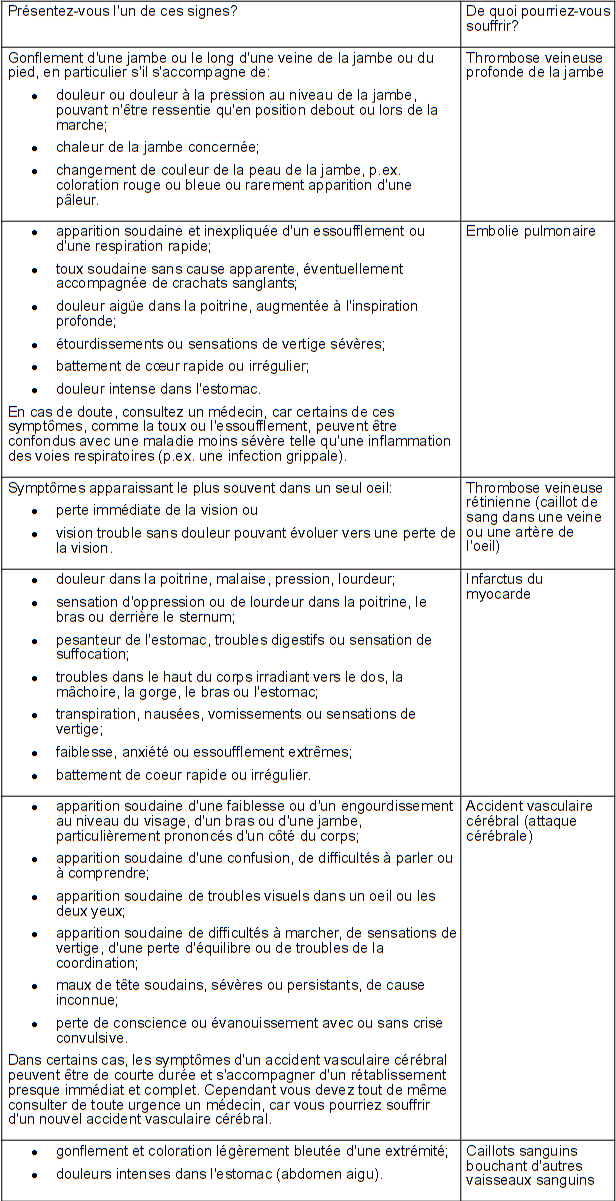
Quand le risque de caillot sanguin dans une veine est-il augmenté ?
Le risque de développer une thromboembolie veineuse est le plus élevé au cours de la première année d’utilisation. Ce risque plus élevé existe dès la première prise de Cypestra-35 ou lors de la reprise (après un intervalle d’au moins 4 semaines ou un intervalle plus long sans traitement). Les données d’une grande étude indiquent que ce risque élevé existe surtout pendant les 3 premiers mois.
Le risque diminue après la première année, mais reste toujours légèrement plus élevé que si vous ne prenez pas Cypestra-35.
Si vous arrêtez de prendre Cypestra-35, le risque de caillot sanguin revient à la normale en quelques semaines.
Quel est le risque de formation d’un caillot sanguin ?
Le risque global de caillot sanguin dans une jambe ou un poumon est faible avec Cypestra-35, mais est beaucoup plus élevé que chez les femmes ne prenant pas Cypestra-35:
– Sur 10’000 femmes qui ne sont pas enceintes et n’utilisent pas de contraceptif hormonal combiné ou Cypestra-35, environ 2 souffrent d’un caillot sanguin sur une période d’un an.
– Le risque de formation d’un caillot sanguin varie selon vos antécédents médicaux personnels (voir le paragraphe suivant «Facteurs augmentant le risque de caillot sanguin dans une veine»).
Facteurs augmentant le risque de caillot sanguin dans une veine
Le risque de formation de caillot sanguin dans les veines (p.ex. thrombose veineuse profonde, embolie pulmonaire) augmente:
– Avec l’âge (surtout à partir d’environ 35 ans);
– en cas de surcharge pondérale (indice de masse corporelle supérieur à 30 kg/m2);
– avec la survenue antérieure d’un caillot (thrombose de la jambe, embolie pulmonaire ou dans une autre partie du corps), chez un frère ou une soeur ou un parent dans son jeune âge (avant l’âge de 50 ans), ou si vous, ou quelqu’un de votre parenté proche avez des troubles héréditaires de la coagulation connus ou présumés. Dans ce cas, vous devriez consulter un spécialiste avant de commencer à prendre Cypestra-35. Certains facteurs sanguins qui augmentent la tendance aux thromboses veineuses, comme la résistance à la protéine C réactive (mutation du facteur V de Leiden activé par la protéine C réactive), l’homocystéine, le déficit en antithrombine III, le déficit en protéine C, le déficit en protéine S, les anticorps anti-phospholipides (anticorps anti-cardiolipine, anticoagulant lupique). Si l’examen montre des signes de thrombophilie, la prise de Cypestra-35 est contre-indiquée (voir «Quand Cypestra-35 ne doit-il pas être pris ?»);
– si vous souffrez d’un syndrome des ovaires polykystiques (un trouble des ovaires pouvant être associé à des signes d’une influence plus importante des hormones masculines [p.ex. augmentation de la pilosité du visage et du corps] et à un risque élevé de thrombose);
– en cas d’immobilisation de longue durée, d’interventions chirurgicales lourdes, de toute intervention chirurgicale au niveau des jambes ou en cas de jambe dans le plâtre et de blessures graves. Dans ces cas-là, il convient d’arrêter de prendre Cypestra-35 (au moins 4 semaines avant des interventions chirurgicales prévues). Il appartient au médecin de décider du moment où vous pourrez reprendre Cypestra-35 (au plus tôt 2 semaines après mobilisation complète).
D’autres facteurs de risque sont le lupus érythémateux disséminé, le syndrome hémolytique et urémique, la maladie de Crohn, la colite ulcéreuse, l’anémie falciforme et le cancer.
Si vous cumulez plusieurs de ces situations ou si l’une de ces maladies est particulièrement grave, votre risque de formation d’un caillot sanguin peut être encore plus élevé.
Le risque de formation de caillots sanguins est élevé pendant un maximum de 12 semaines suivant un accouchement. C’est pourquoi vous devez demander à votre médecin quand vous pourrez recommencer à prendre Cypestra-35.
Il est important que vous informiez votre médecin si l’une de ces situations vous concerne, même si vous n’en êtes pas certaine. Votre médecin pourra alors décider d’arrêter Cypestra-35.
Quand le risque de caillot sanguin dans une artère est-il augmenté ?
De la même manière qu’un caillot sanguin dans une veine, un caillot dans une artère peut causer de graves problèmes. Il peut par exemple provoquer un infarctus du myocarde ou un accident vasculaire cérébral.
Facteurs augmentant le risque de caillot sanguin dans une artère
Il est important de noter que le risque d’infarctus du myocarde ou d’accident vasculaire cérébral associé à la prise de Cypestra-35 est très faible, mais peut augmenter:
– Avec l’âge (plus de 35 ans);
– si vous fumez. Lors de la prise de Cypestra-35, il est conseillé d’arrêter de fumer. Si vous ne parvenez pas à arrêter de fumer et si vous êtes âgée de plus de 35 ans, votre médecin pourra vous conseiller d’utiliser un autre traitement;
– si vous êtes en surpoids (indice de masse corporelle supérieur à 30 kg/m2);
– si votre pression artérielle est élevée;
– si un membre de votre famille proche a déjà eu un infarctus du myocarde ou un accident vasculaire cérébral à un âge jeune (avant l’âge de 50 ans). Si tel est le cas, le risque que vous ayez un infarctus du myocarde ou un accident vasculaire cérébral pourrait également être plus élevé;
– si vous ou un membre de votre famille proche avez un taux de graisses dans le sang élevé (cholestérol ou triglycérides);
– si vous avez des migraines et en particulier des migraines avec aura;
– si vous souffrez d’un syndrome des ovaires polykystiques (un trouble des ovaires pouvant être associé à des signes d’une influence plus importante des hormones masculines [p. ex. augmentation de la pilosité du visage et du corps] et à un risque élevé de thrombose);
– si vous avez des problèmes cardiaques (maladie d’une valve cardiaque, trouble du rythme appelé fibrillation auriculaire);
– si vous êtes diabétique;
– si vous avez un lupus érythémateux disséminé (LED – une maladie diminuant votre système de défense naturel).
Si vous cumulez plusieurs de ces situations ou si l’une de ces maladies est particulièrement grave, votre risque de formation d’un caillot sanguin peut être encore plus élevé.
Si l’une des situations susmentionnées change pendant la période où vous prenez Cypestra-35, par exemple si vous commencez à fumer, si un membre de votre famille proche présente une thrombose sans raison connue ou si vous prenez beaucoup de poids, informez-en votre médecin.
Maladies tumorales
Une fréquence légèrement plus élevée de cancer du sein a été constatée chez les femmes qui utilisent des préparations hormonales combinées telles que Cypestra-35, par rapport aux femmes du même âge qui n’utilisent pas de telles préparations. Cette différence disparaît toutefois 10 ans après l’arrêt de ces préparations. On ignore si la différence est due à ces préparations elles-mêmes. Il se peut que ces femmes aient juste fait l’objet d’un examen plus soigneux et plus fréquent, d’où le dépistage plus précoce du cancer du sein.
Après une utilisation prolongée de substances hormonales telles que celles contenues dans Cypestra-35, on a observé dans de rares cas des modifications hépatiques bénignes, plus rarement malignes, dont les complications peuvent conduire à des hémorragies internes et imposer l’arrêt de la préparation. Aussi est-il important d’aviser votre médecin si vous ressentez des douleurs épigastriques inhabituelles qui ne disparaissent pas rapidement spontanément.
Chez les femmes qui utilisent des préparations hormonales combinées telles que Cypestra-35 pendant une période prolongée, les cas de cancer du col de l’utérus sont plus fréquents. Le risque le plus élevé de cancer du col utérin est associé à une infection prolongée à papillomavirus (infection à VHP). La prise prolongée de Cypestra-35 peut éventuellement contribuer à l’augmentation de ce risque.
Les tumeurs susmentionnées peuvent mettre la vie en danger ou être mortelles.
Les hormones que contient Cypestra-35 peuvent influencer les résultats de certaines analyses de sang. Informez donc votre médecin que vous prenez Cypestra-35 lorsque l’on vous fait une analyse de sang.
Cypestra-35 contient du lactose et du saccharose. Si votre médecin vous a informé(e) d’une intolérance à certains sucres, contactez-le avant de prendre Cypestra-35.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dragée, c.-à-d. qu’il est essentiellement «sans sodium».
Affections psychiatriques
Certaines femmes utilisant des contraceptifs hormonaux tels que Cypestra-35 ont rapporté des dépressions ou des états dépressifs. Les dépressions peuvent avoir une évolution grave et occasionnellement engendrer des idées suicidaires. Si vous présentez des variations de l’humeur et des symptômes dépressifs, demandez conseil à un médecin le plus rapidement possible.
Interactions avec d’autres médicaments
L’effet de Cypestra-35 peut être diminué par la prise simultanée de certains médicaments. Ceux-ci comprennent des médicaments destinés au traitement:
– De l’épilepsie (primidone, phénytoïne, barbituriques, carbamazépine, oxcarbazépine, topiramate, felbamate);
– de la tuberculose (rifampicine, rifabutine);
– des infections provoquées par le VIH et le virus de l’hépatite C (dits inhibiteurs de protéases et inhibiteurs non nucléosidiques de la transcriptase inverse);
– des mycoses (griséofulvine);
– de l’hypertension artérielle dans les artères pulmonaires, tels que le bosentan;
– de la narcolepsie, tels que le modafinil;
– de certaines infections nécessitant la prise prolongée (pendant plus de 10 jours) d’antibiotiques (tétracyclines);
– des états dépressifs (préparations à base de millepertuis (voir ci-dessous)).
Si vous utilisez l’un des médicaments susmentionnés sur une courte durée (pendant 10 jours au maximum), vous pouvez continuer à prendre Cypestra-35. Vous devez cependant utiliser des méthodes contraceptives supplémentaires non hormonales, p.ex. des préservatifs pendant le traitement et les 28 jours suivant l’arrêt de ce médicament. Demandez conseil à votre médecin ou à votre pharmacien. Si le traitement simultané est poursuivi au-delà de la fin de la plaquette actuelle de Cypestra-35, il vous faudra commencer la plaquette suivante sans interruption, donc sans la pause habituelle (voir «Comment utiliser Cypestra-35 ?»). Votre médecin vous donnera les instructions nécessaires.
Veuillez vous informer auprès de votre médecin ou votre pharmacien sur la conduite à tenir si vous devez prendre pendant une longue durée (c.-à-d. pendant plus de 10 à 14 jours) des antibiotiques (p.ex. en cas d’inflammations osseuses ou de borréliose).
Lorsque vous prenez Cypestra-35, vous ne devez pas prendre simultanément une préparation contre les dépressions à base de millepertuis (Hypericum), car l’effet contraceptif peut s’en trouver diminué. Des cas de saignements entre les règles et des cas isolés de grossesse non désirée ont été rapportés.
Certains médicaments ainsi que le jus de pamplemousse peuvent augmenter la concentration des principes actifs de Cypestra-35 dans le sang. Informez votre médecin si vous prenez du jus de pamplemousse ou l’un des médicaments suivants:
– Médicaments contre les mycoses qui contiennent des principes actifs tels que p.ex. l’itraconazole, le voriconazole ou le fluconazole;
– certains antibiotiques (macrolides) qui contiennent comme principe actif la clarithromycine ou l’érythromycine;
– certains médicaments pour traiter des maladies cardio-vasculaires (contenant les principes actifs diltiazem ou vérapamil);
– analgésiques et anti-inflammatoires qui contiennent comme principe actif l’étoricoxib;
– médicaments diminuant les taux élevés de cholestérol dans le sang qui contiennent comme principe actif l’atorvastatine ou la rosuvastatine.
Si vous êtes diabétique, la prise de Cypestra-35 peut modifier vos besoins en médicaments hypoglycémiants (dont l’insuline).
Cypestra-35 peut également influencer l’action d’autres médicaments, soit en l’accentuant soit en la diminuant. Ceci concerne p.ex. la ciclosporine, la mélatonine, la tizanidine, la théophylline et l’antiépileptique lamotrigine (comme ceci pourrait provoquer une augmentation de la fréquence des crises convulsives, votre médecin surveillera le taux sanguin de lamotrigine au début de la prise de Cypestra-35 et lors de l’arrêt de Cypestra-35). Mais d’autres médicaments peuvent aussi être concernés, tels que des antalgiques, des antidépresseurs, des médicaments contre le paludisme, des calmants, des médicaments pour le coeur, des produits à base de cortisone et des anticoagulants.
Ne prenez pas Cypestra-35 si vous avez une hépatite C et si vous prenez l’association à base des principes actifs ombitasvir/paritaprévir/ritonavir utilisée avec ou sans dasabuvir, glécaprévir/pibrentasvir ou sofosbuvir/velpatasvir/voxilaprévir, car ceci entraîne une augmentation des valeurs hépatiques dans le sang (augmentation de l’enzyme hépatique ALAT). Cypestra-35 peut être à nouveau pris uniquement lorsque les paramètres de la fonction hépatique sont revenus à la normale. Consultez votre médecin pour savoir quand vous pouvez commencer à reprendre Cypestra-35 après l’arrêt de cette association à base de ces principes actifs.
En raison des interactions possibles avec d’autres médicaments, il est important d’informer tous les autres médecins et dentistes consultés et notamment le médecin ou le dentiste qui vous prescrit un autre médicament, que vous utilisez Cypestra-35.
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie
– vous êtes allergique
– vous prenez déjà d’autres médicaments ou utilisez déjà d’autres médicaments en usage externe (même en automédication!).
Effet sur l’aptitude à la conduite et l’utilisation de machines
Aucune étude portant sur l’aptitude à la conduite et à l’utilisation de machines n’a été effectuée.
Cypestra-35 peut-il être pris pendant la grossesse ou l’allaitement ?
Cypestra-35 ne doit pas être pris pendant la grossesse ou en cas de suspicion de grossesse.
L’éventualité d’une grossesse devra être exclue avant le début de la prise de Cypestra-35.
Si vous devenez enceinte pendant la prise de Cypestra-35, vous devez cesser immédiatement la prise du médicament et consulter le médecin.
Si vous allaitez, vous ne devez pas prendre Cypestra-35, la qualité et la quantité du lait maternel pouvant être affectées et les principes actifs pouvant passer en faibles quantités dans le lait maternel.
Comment utiliser Cypestra-35 ?
Ne changez pas de votre propre chef le dosage prescrit. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Il faut arrêter les autres contraceptifs hormonaux pris précédemment.
Durée du traitement
Trois mois au moins sont nécessaires pour obtenir un soulagement des symptômes. La durée du traitement est fonction du degré de gravité des symptômes de la maladie (manifestations d’androgénisation) et de leur réponse au traitement; en général, elle est de plusieurs mois.
Votre médecin contrôlera régulièrement s’il est indiqué de poursuivre le traitement. En outre, Cypestra-35 ne doit pas continuer à être pris exclusivement comme contraceptif. Si les symptômes dépendant des hormones masculines réapparaissent après l’arrêt, le traitement par Cypestra-35 pourra être repris après consultation de votre médecin.
Début de la prise
La plaquette-calendrier contient 21 dragées. Un jour de la semaine est indiqué pour chaque dragée de la plaquette. Prélevez la première dragée de la plaquette-calendrier, à l’endroit marqué du jour de la semaine correspondant (p.ex. «Lun» pour lundi), en la faisant passer par pression à travers le feuillet d’aluminium, et avalez-la sans la croquer avec du liquide. L’heure de la prise importe peu, cependant vous devrez vous en tenir une fois pour toutes à l’heure que vous aurez choisie. Suivez le sens des flèches jusqu’à ce que vous ayez pris toutes les 21 dragées. Ne prenez aucune dragée pendant les 7 jours suivants. Vos règles (hémorragie de privation) devraient survenir pendant ces 7 jours, 2 à 3 jours après la prise de la dernière dragée. Commencez la plaquette suivante de Cypestra-35 le 8e jour, même si les saignements persistent encore. Cela signifie que vous commencerez chaque nouvelle plaquette de Cypestra-35 toujours le même jour de la semaine, comme lors de la première plaquette et que vos règles commenceront également à peu près le même jour de la semaine, chaque mois.
Si vous n’avez pas pris de contraceptif hormonal le mois précédent
Attendez vos prochaines règles. Commencez la prise des dragées le 1er jour du cycle (1er jour des règles = 1er jour du cycle).
Le 1er cycle sera un peu raccourci, tandis que tous les cycles suivants dureront quatre semaines.
Vous pouvez aussi commencer la prise des dragées du 2e au 5e jour de votre cycle, mais vous devrez alors utiliser des méthodes contraceptives supplémentaires (contraceptifs non hormonaux, à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures) pendant les 7 premiers jours de la prise durant le premier cycle.
Si vous preniez jusque-là un contraceptif combiné de 21 jours («pilule», patch transdermique ou anneau vaginal)
Commencez la prise de Cypestra-35 de préférence le lendemain de la prise de la dernière dragée/du dernier comprimé de la pilule prise jusqu’ici (c.-à-d. sans faire de pause). Vous pouvez aussi commencer la prise de Cypestra-35 plus tard, mais au plus tard le lendemain des 7 jours habituels de pause de votre pilule actuelle. En cas de patch transdermique ou d’anneau vaginal, il faut commencer la prise de Cypestra-35 le jour du retrait du dernier anneau ou du dernier patch et au plus tard le jour où le patch ou l’anneau vaginal suivants devrait être utilisé.
Si vous preniez jusque-là une pilule combinée de 28 jours (plaquette comprenant 21 à 24 comprimés contenant le principe actif et 4 à 7 comprimés dépourvus de principe actif)
Commencez immédiatement (c.-à-d. sans faire de pause) la prise de la première dragée de Cypestra-35 dès le lendemain de la prise du dernier comprimé contenant le principe actif de l’ancienne plaquette (soit après 21 à 24 jours). Vous pouvez cependant aussi attendre vos prochaines règles et commencer la prise de Cypestra-35 le lendemain de la prise du dernier comprimé sans principe actif.
Si vous preniez jusque-là une monopilule progestative (minipilule)
Vous pouvez arrêter la prise de la minipilule n’importe quel jour et commencer la prise de Cypestra-35 le lendemain à la même heure. Vous devez cependant utiliser une méthode contraceptive supplémentaire non hormonale (à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures) pendant les 7 premiers jours de la prise de Cypestra-35.
Si vous utilisiez jusque-là une injection d’hormones, un implant ou un stérilet libérant un progestatif
Commencez la prise de Cypestra-35 le jour où vous devriez faire votre prochaine injection ou le jour où l’on vous retire votre implant ou votre stérilet. Utilisez toutefois une méthode contraceptive supplémentaire (à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures) pendant les 7 premiers jours de la prise de Cypestra-35.
Après une fausse couche ou une interruption de grossesse survenue dans les 3 premiers mois de la grossesse
Vous pouvez commencer immédiatement la prise de Cypestra-35 et vous n’avez pas besoin de recourir à une méthode contraceptive supplémentaire. Prenez toutefois l’avis de votre médecin.
Après un accouchement ou une interruption de grossesse survenue au-delà des 3 premiers mois de grossesse
Après un accouchement ou une interruption de grossesse survenue au-delà des 3 premiers mois de grossesse, la prise de Cypestra-35 ne devrait commencer au plus tôt qu’entre le 21e et le 28e jour. Vous n’avez alors pas besoin de recourir à une méthode contraceptive supplémentaire. Si plus de 28 jours se sont écoulés depuis l’accouchement, vous devrez toutefois utiliser une méthode contraceptive supplémentaire pendant les 7 premiers jours. Si vous avez eu auparavant des rapports sexuels, il vous faut exclure l’éventualité d’une grossesse ou attendre le début de vos prochaines règles avant de commencer la prise de Cypestra-35. Veuillez observer que vous ne devez pas prendre Cypestra-35 si vous allaitez (voir «Cypestra-35 peut-il être pris pendant la grossesse ou l’allaitement ?»).
Le risque de formation de caillots sanguins est élevé pendant un maximum de 12 semaines après un accouchement. C’est pourquoi vous devez demander à votre médecin quand vous pouvez recommencer à prendre Cypestra-35.
Si vous avez oublié de prendre la dragée du jour
S’il s’est écoulé moins de 12 heures depuis le moment où vous auriez dû prendre la dragée, la fiabilité de la contraception est encore assurée. Vous devez alors prendre immédiatement la dragée oubliée et continuer à prendre quotidiennement les dragées suivantes à l’heure habituelle.
Si vous avez oublié de prendre la dragée depuis plus de 12 heures, il se peut que la protection contraceptive ne soit plus complète. Plus vous avez oublié de dragées, plus le risque est grand que la protection contraceptive ne soit plus assurée. Le risque de devenir enceinte est particulièrement élevé si vous oubliez de prendre des dragées au début ou à la fin de la plaquette. C’est pourquoi vous devez observer les règles suivantes:
Si vous avez oublié plus d’une dragée d’une plaquette
Demandez conseil à votre médecin.
Si vous avez oublié 1 dragée dans la 1re semaine de la prise
Prenez la dragée oubliée sitôt que vous vous êtes aperçue de votre oubli – même si cela implique la prise rapprochée de 2 dragées l’une après l’autre le même jour – et prenez les dragées suivantes chaque jour à l’heure habituelle.
Pendant les 7 prochains jours, il vous faudra utiliser une méthode contraceptive supplémentaire non hormonale (à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures). Si vous avez déjà eu un rapport sexuel dans la semaine ayant précédé l’oubli de la prise, il se peut que vous soyez enceinte. Informez-en immédiatement votre médecin.
Si vous avez oublié 1 dragée dans la 2esemaine de la prise
Prenez la dragée oubliée sitôt que vous vous apercevez de votre oubli – même si cela implique la prise rapprochée de 2 dragées l’une après l’autre le même jour – et prenez les dragées suivantes chaque jour à l’heure habituelle.
La protection contraceptive est conservée à condition que la prise ait été régulière pendant les 7 jours précédents. Vous n’avez pas besoin d’utiliser de contraceptif supplémentaire non hormonal. Si cela n’est pas le cas, utilisez une méthode contraceptive supplémentaire non hormonale (à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures).
Si vous avez oublié 1 dragée dans la 3e semaine de la prise
Vous pouvez choisir une des deux possibilités suivantes, sans avoir à utiliser un contraceptif supplémentaire si la prise de Cypestra-35 a été régulière pendant les 7 jours précédents. Sinon, suivez la première des deux possibilités et utilisez une méthode contraceptive supplémentaire non hormonale (à l’exclusion de l’abstinence périodique selon Ogino-Knaus et de la méthode des températures) pendant les 7 jours suivants.
Prenez la dragée oubliée sitôt que vous vous apercevez de votre oubli – même si cela implique la prise rapprochée de 2 dragées l’une après l’autre le même jour – et prenez les dragées suivantes chaque jour à l’heure habituelle. Commencez la prise des dragées de la plaquette suivante immédiatement après la fin de la dernière plaquette, c.-à-d. sans observer la pause de 7 jours. L’hémorragie de privation habituelle ne se produira pas; de petites pertes sanglantes (spotting) ou des saignements intermédiaires pourront toutefois être plus fréquents jusqu’à ce que vous ayez pris toutes les dragées de cette deuxième plaquette.
Ou:
Ne prenez plus d’autres dragées. Après une pause de 7 jours au maximum, le jour de l’oubli de la dragée compris, reprenez la prise des dragées en commençant la plaquette suivante. Cette méthode permet aussi de recommencer la prise le même jour de la semaine que jusqu’alors.
Si vous avez oublié des dragées et que vos règles ne surviennent pas pendant la première pause de 7 jours, il se peut que vous soyez enceinte. Consultez donc votre médecin avant de reprendre la plaquette suivante.
Mesures de sécurité en cas de vomissements ou de troubles gastro-intestinaux
En cas de troubles gastro-intestinaux sévères, l’organisme n’absorbe probablement pas complètement les composants actifs de la dragée. La protection contraceptive peut donc être diminuée, comme lors de l’oubli d’une dragée.
Si vous vomissez dans les 3 à 4 heures suivant la prise des dragées de Cypestra-35, il faut suivre les conseils donnés dans le cas de l’oubli d’une dragée. Afin que le schéma habituel de la prise puisse être conservé, il vous faut prendre la dragée supplémentaire d’une plaquette de réserve.
Si vous désirez retarder vos règles
Vous pouvez décaler vos règles en commençant la prise de la plaquette suivante de Cypestra-35 dès que vous avez terminé la plaquette actuelle, sans observer la pause de 7 jours. Vous pouvez poursuivre la prise aussi longtemps que vous le désirez, au maximum cependant jusqu’à la fin de cette deuxième plaquette. Lorsque vous désirez avoir vos règles, arrêtez la prise. Lors de la prise de la deuxième plaquette, il se peut que de petites pertes sanglantes (spotting) ou des saignements intermédiaires surviennent. Commencez la plaquette suivante après la pause habituelle de 7 jours.
Si vous désirez que vos règles commencent généralement un autre jour de la semaine
Si vous prenez les dragées selon les instructions, vos règles se produiront toutes les 4 semaines à peu près le même jour de la semaine. Si vous désirez changer celui-ci, raccourcissez simplement (ne prolongez jamais) la prochaine pause. Si vos règles commencent habituellement le vendredi et que vous désirez à l’avenir que ce soit le mardi (3 jours plus tôt), prenez la première dragée de la plaquette suivante trois jours plus tôt que d’habitude. Si l’intervalle est très court (p.ex. 3 jours ou moins), il se peut que l’hémorragie de privation ne se produise pas. De petites pertes sanglantes (spotting) ou des saignements intermédiaires sont cependant possibles pendant la prise de la prochaine plaquette.
Conduite à tenir en cas d’irrégularité des saignements
Lors de la prise de préparations hormonales combinées telles que Cypestra-35 et particulièrement pendant les premiers mois de la prise, des saignements inhabituels (petites pertes sanglantes ou saignements intermédiaires) peuvent se produire. Il se peut que vous ayez besoin de serviettes périodiques ou de tampons, mais la prise des dragées ne doit pas être interrompue.
Les saignements intermenstruels légers cessent généralement dès que le corps s’est habitué à la prise de Cypestra-35 (normalement après 3 cycles environ). Consultez votre médecin en cas de saignements persistants, forts, similaires à la menstruation normale ou répétés.
Conduite à tenir en cas d’absence de règles
L’hémorragie de privation peut faire défaut au cours de la pause sans prise de dragées. Si vous avez pris les dragées correctement, que vous n’avez pas eu de vomissements et que vous n’avez pas pris d’autres médicaments, la probabilité d’une grossesse est extrêmement faible. Prenez Cypestra-35 comme d’habitude.
Si les règles font défaut deux fois de suite, il se peut que vous soyez enceinte. Consultez sans délai votre médecin. Ne poursuivez pas la prise de Cypestra-35 tant que votre médecin n’a pas exclu une grossesse.
Après l’arrêt de Cypestra-35, les glandes génitales reprennent en général leur pleine fonction et l’aptitude à concevoir est normale. Le premier cycle est généralement allongé d’une semaine environ. Si toutefois le déroulement du cycle ne redevenait pas normal au cours des 2 à 3 premiers mois, veuillez consulter votre médecin.
Si vous ne voulez pas être enceinte après l’arrêt de Cypestra-35, demandez à votre médecin de vous conseiller d’autres méthodes contraceptives.
Enfants et adolescents
L’efficacité et la sécurité de l’acétate de cyprotérone et de l’éthinylestradiol ont essentiellement été examinées chez des femmes adultes. Chez les adolescentes, le dosage recommandé sera le même que chez les adultes (sur prescription médicale). Cypestra-35 ne doit pas être pris chez les jeunes filles avant la puberté.
Quels effets secondaires Cypestra-35 peut-il provoquer ?
Veuillez informer votre médecin de tous les événements indésirables, en particulier des symptômes sévères ou persistants ou des modifications de votre état de santé si vous soupçonnez Cypestra-35 d’en être à l’origine.
Toutes les femmes prenant Cypestra-35 présentent un risque élevé de caillots sanguins dans les veines (thromboembolie veineuse) ou les artères (thromboembolie artérielle).
La probabilité que vous présentiez un caillot sanguin peut être élevée si vous souffrez d’une autre maladie augmentant ce risque (pour de plus amples informations sur les maladies augmentant le risque de caillots sanguins et sur les symptômes d’un caillot sanguin, voir «Effets sur la coagulation sanguine, risque de maladies vasculaires» dans la rubrique «Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?»).
Les autres réactions sévères liées à la prise de Cypestra-35 ainsi que les symptômes qui y sont associés sont décrits dans le paragraphe «Maladies tumorales» de la rubrique «Quelles sont les précautions à observer lors de la prise de Cypestra-35 ?». Veuillez lire ces paragraphes et consulter sans délai votre médecin si vous croyez que vous souffrez d’un de ces troubles.
La prise de Cypestra-35 peut provoquer les autres effets secondaires suivants:
Fréquent (concerne 1 à 10 utilisatrices sur 100)
Prise de poids, états dépressifs, altérations de l’humeur, maux de tête, troubles gastro-intestinaux, nausées, éruptions cutanées, tensions ou douleurs dans les seins.
Occasionnel (concerne 1 à 10 utilisatrices sur 1000)
Rétention de liquide dans les tissus, baisse de la libido, migraine, vomissements, diarrhée, formation de papules sur la peau, chloasma (marques brunâtres sur le visage), augmentation de volume des seins, saignements entre les règles et absence de règles.
Rare (concerne 1 à 10 utilisatrices sur 10’000)
Réactions d’hypersensibilité, perte de poids, altérations du métabolisme du glucose, augmentation de la libido, vertige, augmentation des crises épileptiques, crampes dans les jambes, problèmes lors du port de lentilles de contact, hausse de la tension artérielle, affections thromboemboliques artérielles et veineuses (p.ex. thrombose veineuse, embolie pulmonaire, attaque cérébrale, infarctus du myocarde), tumeurs au foie, hépatite (inflammation du foie), jaunisse, aggravation d’une porphyrie (modification du métabolisme de l’hémoglobine), réactions cutanées sévères, démangeaisons, écoulement mammaire, pertes vaginales et augmentation de la fréquence d’infections (surtout de mycoses) vaginales, caillot sanguin dans une veine ou une artère, p.ex.:
– Dans une jambe ou un pied;
– dans un poumon;
– infarctus du myocarde;
– accident vasculaire cérébral;
– mini-accident vasculaire cérébral ou symptômes passagers ressemblant à un accident vasculaire cérébral, appelés accidents ischémiques transitoires (AIT);
– caillot sanguin dans le foie, l’estomac/intestin, les reins ou l’oeil.
Très rare (concerne moins d’une utilisatrice sur 10’000)
Troubles auditifs.
En outre, les symptômes et maladies rapportés lors de l’utilisation d’autres préparations hormonales combinées ont été les suivants: maladies herpétiques, formation de nodules dans le sein, cancer du sein, dysplasie cervicale (modification de la muqueuse du col de l’utérus), cancer du col de l’utérus, augmentation des graisses dans le sang, perte de l’audition, modifications bénignes du foie, acné, chute de cheveux, troubles menstruels, infections vaginales, myomes (tumeurs bénignes de l’utérus), rétention de liquide dans les tissus (p.ex. jambes enflées).
Si vous remarquez des effets secondaires, veuillez en informer votre médecin, votre pharmacien. Ceci vaut en particulier pour les effets secondaires non mentionnés dans cette notice d’emballage.
À quoi faut-il encore faire attention ?
Ce médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Remarques concernant le stockage
Ne pas conserver au-dessus de 30°C. Conserver à l’abri de la lumière dans l’emballage d’origine.
Conserver hors de la portée des enfants.
Remarques complémentaires
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien qui disposent d’une information détaillée destinée aux professionnels.
Que contient Cypestra-35 ?
Principes actifs
1 dragée contient comme principes actifs 2 mg d’acétate de cyprotérone et 0.035 mg d’éthinylestradiol.
Excipients
Noyau du comprimé: Lactose monohydraté, cellulose microcristalline, povidone K-30, croscarmellose sodique, stéarate de magnésium.
Enrobage du comprimé: Hypromellose, dioxyde de titane (E171), macrogol 400, indigotine (E132), oxyde de fer jaune, rouge et noir (E172), jaune de quinoléine (E104), éthanol, gomme- laque, cire de carnauba jaune, cire d’abeille blanchie, saccharose.
Numéro d’autorisation
57225 (Swissmedic).
Où obtenez-vous Cypestra-35 ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Il est disponible en plaquettes-calendrier de 21 dragées et de 3× 21 dragées.
Titulaire de l’autorisation
Mepha Pharma AG, Basel.
Cette notice d’emballage a été vérifiée pour la dernière fois en août 2021 par l’autorité de contrôle des médicaments (Swissmedic).
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 10.12.2021, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans le paragraphe en gras juste ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère mise à jour de cette page depuis le lancement début 2021 de cette rubrique. MAJ 1 ( 10.12.2021 )
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


