Teriparatid Zentiva®
ATTENTION SELON SWISSMEDIC (EDITION DE FEVRIER 2024), CE MEDICAMENT EST HORS COMMERCE (EXTINCTION DE L’AUTORISATION) EN SUISSE DEPUIS LE 26.03.2024
Information destinée aux patients en Suisse
Qu’est-ce que Teriparatid Zentiva et quand est-il utilisé ?
Teriparatid Zentiva appartient à une nouvelle classe de médicaments induisant la formation de tissus osseux. Son principe actif, le tériparatide, est une hormone qui agit sur le métabolisme osseux. Il est produit synthétiquement. La partie active de cette substance est identique à la parathormone naturelle.
Teriparatid Zentiva est un médicament délivré sur ordonnance médicale et destiné au traitement de l’ostéoporose. L’ostéoporose est une maladie dans laquelle les os se fragilisent. Cette maladie affecte très souvent les femmes après la ménopause mais elle peut aussi toucher les hommes. Bien qu’aucun symptôme ne se manifeste initialement, une ostéoporose non traitée augmente les risques de fracture osseuse, avant tout de la colonne vertébrale, de la hanche et du poignet. En outre, des douleurs dorsales, une diminution de la taille du corps et un dos qui s’arrondit sont des conséquences possibles.
L’ostéoporose se développe également souvent chez les patients traités par des corticostéroïdes.
Teriparatid Zentiva stimule la formation des os, renforce les os et réduit ainsi le risque de fracture osseuse.
On utilise Teriparatid Zentiva pour le traitement de l’ostéoporose chez les femmes après la ménopause qui présentent un risque élevé de fractures osseuses et chez les hommes qui présentent un risque important de fractures osseuses. Teriparatid Zentiva est aussi utilisé chez des adultes souffrant d’ostéoporose qui sont traités ou ont été traités avec des glucocorticoïdes.
Teriparatid Zentiva vous a été prescrit personnellement et vous ne devez jamais donner votre stylo Teriparatid Zentiva pré-rempli à d’autres personnes, même si elles ont les mêmes symptômes que vous.
De quoi faut-il tenir compte en dehors du traitement ?
Lors d’études faites sur des rats dans le cadre du développement et de contrôles du médicament, quelques animaux, ayant reçu Teriparatid Zentiva toute leur vie, ont développé un cancer des os (ostéosarcome). Chez les êtres humains, l’ostéosarcome est un cancer grave mais très rare (env. 4/1’000’000 par an). On ignore quelle est l’importance de cette découverte pour l’être humain; ni lors d’essais cliniques, ni durant la période d’observation qui a suivi le traitement, on n’a observé d’ostéosarcomes.
Quand Teriparatid Zentiva ne doit-il pas être utilisé ?
Vous ne devez pas prendre Teriparatid Zentiva,
– si vous souffrez de la maladie de Paget.
– si vous avez un taux élevé inexpliqué de phosphatases alcalines dans le sang, lequel signifie que vous pourriez avoir la maladie de Paget. Si vous avez des doutes, veuillez interroger votre médecin.
– si vous souffrez d’une maladie rénale grave.
– si vous êtes un enfant ou un adolescent âgé de moins de 18 ans.
– si on a diagnostiqué chez vous un cancer des os ou tout autre type de cancer qui se serait aussi étendu à vos os (métastases).
– si vous avez subi une radiothérapie qui a aussi concerné vos os (squelette).
– si vous souffrez de certaines maladies des os. Si vous avez une maladie des os, veuillez en informer votre médecin.
– si vous avez trop de calcium dans le sang (une hypercalcémie).
– si vous êtes allergique au principe actif de Teriparatid Zentiva (tériparatide) ou à l’un de ses composants particuliers.
– si vous êtes enceinte ou si vous allaitez.
Quelles sont les précautions à observer lors de l’utilisation de Teriparatid Zentiva ?
Veuillez informer votre médecin ou votre pharmacien si vous prenez d’autres médicaments ou que vous en avez pris jusqu’à récemment, car cela pourrait provoquer des interactions.
Certains patients peuvent ressentir une sensation de vertige après l’injection de Teriparatid Zentiva. Si vous ressentez cette sensation de vertige, vous ne devez pas conduire ni utiliser des machines jusqu’à ce que vous vous sentiez mieux.
Ce médicament contient moins de 1 mmol (23 mg) de sodium par dose, c.-à-d. qu’il est essentiellement «sans sodium».
Veuillez informer votre médecin ou votre pharmacien si
– vous souffrez d’une autre maladie
– vous êtes allergique ou
– vous prenez déjà d’autres médicaments en usage interne ou externe (même en automédication)!
Teriparatid Zentiva peut-il être utilisé pendant la grossesse ou l’allaitement ?
Grossesse
N’utilisez pas Teriparatid Zentiva si vous êtes enceinte.
Allaitement
N’utilisez pas Teriparatid Zentiva si vous allaitez.
Comment utiliser Teriparatid Zentiva ?
Utilisez toujours Teriparatid Zentiva conformément aux instructions du médecin. Si vous avez des doutes, prenez conseil auprès de votre médecin ou de votre pharmacien.
La solution injectable de Teriparatid Zentiva est disponible dans un stylo. Le stylo ne doit être utilisé que pour votre traitement personnel et ne doit jamais servir au traitement d’autres personnes. N’utilisez pas non plus le stylo d’une autre personne car des maladies pourraient éventuellement être transmises entre patients par le biais du stylo. Votre médecin, le personnel soignant ou votre pharmacien vous expliquera comment utiliser votre stylo Teriparatid Zentiva. Pour votre propre information concernant l’utilisation du stylo Teriparatid Zentiva, veuillez aussi lire attentivement son mode d’emploi avant de commencer le traitement. Pour le cas où il y aurait de nouvelles informations disponibles, nous vous recommandons de lire le mode d’emploi et l’information destinée aux patients chaque fois que vous recevrez un nouvel emballage.
La dose habituelle de Teriparatid Zentiva est de 20 µg par jour. On injecte Teriparatid Zentiva par voie sous-cutanée (sous la peau) dans la cuisse ou dans la peau du ventre. Teriparatid Zentiva peut être utilisé à tout moment de la journée, indépendamment des repas.
La durée du traitement est de 24 mois au maximum. Le traitement avec Teriparatid Zentiva de 24 mois ne doit pas être répété.
Il est recommandé que, durant le traitement avec Teriparatid Zentiva, vous preniez des préparations à base de calcium et/ou de vitamine D. Demandez à votre médecin combien de calcium et de vitamine D vous devriez prendre chaque jour.
Pour ne pas oublier votre injection quotidienne de Teriparatid Zentiva, le mieux est de la faire chaque jour à la même heure.
Si vous avez oublié ou s’il ne vous a pas été possible de vous faire votre injection à l’heure habituelle, rattrapez-la aussi vite que possible le même jour. Ne vous faites pas plus d’une injection par jour.
Si par mégarde vous vous êtes administré plus de Teriparatid Zentiva que prévu, prenez contact avec votre médecin ou avec votre pharmacien.
N’interrompez pas le traitement de Teriparatid Zentiva sans en avoir préalablement parlé avec votre médecin.
Comme décrit dans le mode d’emploi, faites-vous chaque fois des injections tout de suite après avoir sorti Teriparatid Zentiva du réfrigérateur. Remettez le stylo au réfrigérateur immédiatement après usage. Utilisez une nouvelle aiguille à chaque injection. Ne conservez pas le stylo avec une aiguille montée car de la solution pourrait s’échapper du stylo et des bulles d’air se former dans la cartouche.
Teriparatid Zentiva contient une solution stérile, limpide et incolore. N’utilisez pas Teriparatid Zentiva s’il contient des particules solides ou si la solution est trouble ou colorée.
Ne changez pas de votre propre chef la posologie prescrite. Adressez-vous à votre médecin ou à votre pharmacien si vous estimez que l’efficacité du médicament est trop faible ou au contraire trop forte.
Quels effets secondaires Teriparatid Zentiva peut-il provoquer ?
L’utilisation de Teriparatid Zentiva peut provoquer les effets secondaires suivants: nausées et crampes dans les jambes ou dans le dos.
Après l’injection des réactions allergiques à type d’essoufflement, de gonflement du visage, d’éruption cutanée et de douleur dans la poitrine peuvent se produire (rares). Ces réactions allergiques peuvent potentiellement mettre en jeu le pronostic vital.
Si ce type de réactions devait se produire, prenez immédiatement contact avec votre médecin.
Au niveau du site d’injection, il est fréquent d’observer de légères réactions passagères telles qu’une rougeur de la peau, des douleurs, un œdème, des démangeaisons, des hématomes ou un petit saignement.
Dans de très rares cas, de fortes crampes peuvent survenir au niveau du dos.
Si vous avez des vertiges après une injection, asseyez-vous ou allongez-vous jusqu’à ce que vous vous sentiez mieux. Si vous ne ressentez pas d’amélioration, parlez-en à votre médecin avant de poursuivre le traitement.
Prenez contact avec votre médecin si vous souffrez continuellement de nausées, vomissements, constipation, manque d’énergie ou faiblesse musculaire. Ces symptômes peuvent indiquer que la concentration de calcium dans votre sang est trop élevée.
Durant le traitement, votre médecin peut prélever des échantillons de sang et d’urine pour contrôler votre réponse à Teriparatid Zentiva. Votre médecin peut en outre vous demander de faire des examens répétés de votre densité minérale osseuse.
Si vous remarquez d’autres effets secondaires qui ne sont pas décrits ici, veuillez en informer votre médecin ou votre pharmacien.
A quoi faut-il encore faire attention ?
Conservez ce médicament hors de portée des enfants.
Conservez toujours Teriparatid Zentiva au réfrigérateur (2°C-8°C). Ne pas congeler.
Après utilisation, Teriparatid Zentiva doit être replacé immédiatement au réfrigérateur. N’utilisez Teriparatid Zentiva s’il a été congelé.
Après la première utilisation d’un stylo, Teriparatid Zentiva peut être utilisé pendant 28 jours.
Le stylo de Teriparatid Zentiva pré-rempli doit être éliminé comme il se doit au bout de 28 jours, même s’il reste encore de la solution dans le stylo.
La solution injectable soit être limpide et incolore. N’utilisez pas Teriparatid Zentiva si des particules solides se sont formées ou si la solution est trouble ou colorée.
Le médicament ne doit pas être utilisé au-delà de la date figurant après la mention «EXP» sur le récipient.
Pour de plus amples renseignements, consultez votre médecin ou votre pharmacien, qui disposent d’une information détaillée destinée aux professionnels.
Que contient Teriparatid Zentiva ?
Principes actifs
Teriparatid Zentiva contient comme principe actif le tériparatide sous forme d’acétate de tériparatide.
Chaque millilitre de solution injectable contient 250 microgrammes de tériparatide.
Excipients
Acide acétique 99%, acétate de sodium, mannitol, métacrésol, acide chlorhydrique, hydroxyde de sodium et eau pour préparations injectables.
Numéro d’autorisation
68627 (Swissmedic).
Où obtenez-vous Teriparatid Zentiva ? Quels sont les emballages à disposition sur le marché ?
En pharmacie, sur ordonnance médicale.
Il existe des emballages avec 1 stylo prérempli de Teriparatid Zentiva.
Titulaire de l’autorisation
Helvepharm AG, Frauenfeld
Cette notice d’emballage a été vérifiée pour la dernière fois en septembre 2018 par l’autorité de contrôle des médicaments (Swissmedic).
Mode d’emploi de l’injecteur
Vue d’ensemble des pièces de l’injecteur
Teriparatid Zentiva est un médicament que vous recevez dans un injecteur. L’injecteur contient une réserve de médicament pour une injection quotidienne pendant 28 jours consécutifs.
Vous aurez besoin d’une nouvelle aiguille pour chaque injection. Les aiguilles ne sont pas fournies avec l’injecteur.

1.Capuchon de l’injecteur
2.Cartouche contenant le médicament
3.Étiquette
4.Fenêtre de dosage
5.Sélecteur de dose
6.Bouton d’injection
7.Grand capuchon extérieur
8.Petit capuchon intérieur
9.Aiguille
10.Pellicule scellée
Pour votre sécurité
Informations importantes
– Lisez entièrement ce mode d’emploi. Suivez précisément toutes les instructions.
– Lisez la notice d’utilisation du médicament que vous avez reçue avec l’injecteur.
– Si vous avez des questions, adressez-vous à votre médecin, à votre pharmacien/ne ou à votre personnel soignant.
Prévention des infections
– Ne partagez pas votre injecteur avec d’autres personnes, car cela pourrait transmettre des agents pathogènes.
– Utilisez une nouvelle aiguille stérile à chaque injection. Les aiguilles utilisées sont une source d’infection possible.
Utilisation de l’injecteur
– Vérifiez l’étiquette de l’injecteur lorsque vous le sortez du réfrigérateur. Assurez-vous d’utiliser le bon médicament.
– Vérifiez la date de péremption du médicament. N’utilisez pas l’injecteur si la date de péremption est dépassée.
– Veillez à ce que le médicament soit transparent, incolore et exempt de particules.
– Ne transvasez pas le médicament dans une seringue. Teriparatid Zentiva ne doit être injecté qu’avec cet injecteur.
– N’utilisez pas l’injecteur pour plus de 28 injections. Notez la date de la 1re injection dans le journal d’injection au dos du présent mode d’emploi. Déterminez la date de la 28e injection avec un calendrier. Notez également cette date dans le journal d’injection.
– L’injecteur ne peut pas être utilisé par des personnes non voyantes et malvoyantes sans l’aide d’une personne auxiliaire.
Conservation
– Conservez l’injecteur au réfrigérateur, si possible dans le compartiment de la porte.
Procédure en cas de problèmes
– S’il y a eu un problème avec l’injection, ne faites pas d’autre injection le même jour.
– Tenez compte de la section «Que faire si… ?» dans ce mode d’emploi.
– N’utilisez pas l’injecteur s’il est endommagé.
Préparation de l’injecteur avant la première injection
Avant la PREMIÈRE injection, l’injecteur doit être préparé comme décrit ci-après.
Cette étape doit être effectuée une seule fois. Vous n’avez PAS besoin de procéder à ces étapes pour la deuxième injection et les suivantes.
Visser l’aiguille
1.Retirez le capuchon de l’injecteur.
2.Prenez une nouvelle aiguille et enlevez la pellicule scellée du grand capuchon extérieur.
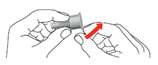
3.Insérez l’aiguille avec le grand capuchon extérieur sur l’injecteur. Tournez ensuite le grand capuchon extérieur dans le sens des aiguilles d’une montre jusqu’à la butée.

4.Retirez le grand capuchon extérieur de l’aiguille et conservez-le pour une utilisation ultérieure.
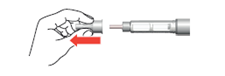
Réglage de la dose
5.Tournez le sélecteur de dose jusqu’à la butée. Assurez-vous que le chiffre «80» est entièrement visible au centre de la fenêtre de dosage et que le repère blanc est visible dans l’évidement de la fenêtre de dosage.
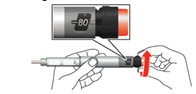
6.Retirez le petit capuchon intérieur de l’aiguille et jetez-le.
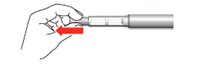
7.Tenez l’injecteur perpendiculairement à l’aiguille vers le haut. Appuyez sur le bouton d’injection jusqu’à la butée et maintenez-le enfoncé pendant 5 secondes. Récupérez le liquide qui s’écoule au moyen d’une lingette à usage unique.
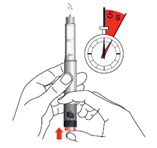
8.Confirmation de la posologie: Assurez-vous que le chiffre «0» est entièrement visible et centré dans la fenêtre de dosage, que la marque blanche est visible dans l’évidement de la fenêtre de dosage et que les deux marques imprimées sur le bouton d’injection et sur l’injecteur coïncident.

Élimination de l’aiguille
Une fois l’injection terminée, retirez l’aiguille car elle pourrait être contaminée.
9.Insérez délicatement l’aiguille dans le grand capuchon extérieur que vous avez conservé.
10.Dévissez l’aiguille en la vissant sur le grand capuchon extérieur dans le sens contraire des aiguilles d’une montre et enlevez l’aiguille de l’injecteur.

11.Éliminez l’aiguille avec le grand capuchon extérieur dans un récipient étanche que vous recevrez dans votre pharmacie ou auprès de votre service de soins.
Tenue du journal d’injection
12.Notez la date du jour et la date de la 28e injection dans le journal d’injection au dos du présent mode d’emploi.
Injection de Teriparatid Zentiva
Préparez-vous pour l’injection
– Lavez-vous les mains avant chaque injection.
– Préparez le site d’injection à la cuisse ou à l’abdomen, comme votre médecin, votre pharmacien/ne ou le personnel soignant vous l’a montré.
– Utilisez une aiguille neuve pour chaque nouvelle injection. Une aiguille usagée présente un risque d’obstruction ou de contamination.
Visser l’aiguille
1.Retirez le capuchon de l’injecteur.
2.Prenez une nouvelle aiguille et enlevez la pellicule scellée du grand capuchon extérieur.

3.Insérez l’aiguille avec le grand capuchon extérieur sur l’injecteur. Tournez ensuite le grand capuchon extérieur dans le sens des aiguilles d’une montre jusqu’à la butée.
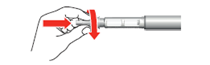
4.Retirez le grand capuchon extérieur de l’aiguille et conservez-le pour une utilisation ultérieure.
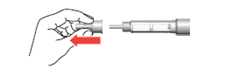
Réglage de la dose
5.Tournez le sélecteur de dose jusqu’à la butée. Assurez-vous que le chiffre «80» est entièrement visible au centre de la fenêtre de dosage et que le repère blanc est visible dans l’évidement de la fenêtre de dosage.
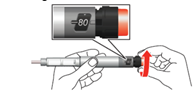
6.Retirez le petit capuchon intérieur de l’aiguille et jetez-le.
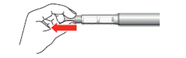
7.Tenez précautionneusement un pli de peau au niveau de la cuisse ou du ventre.
8.Insérez l’aiguille de préférence dans le point d’injection prévu à cet effet à un angle de 90°. Appuyez sur le bouton d’injection jusqu’à la butée et maintenez-le enfoncé pendant 5 secondes. Comptez lentement jusqu’à 5.
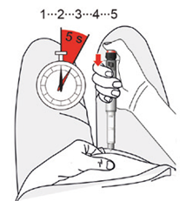
9.Retirez ensuite l’aiguille de la peau.

10.Confirmation de la posologie: Assurez-vous que le chiffre «0» est entièrement visible et centré dans la fenêtre de dosage, que la marque blanche est visible dans l’évidement de la fenêtre de dosage et que les deux marques imprimées sur le bouton d’injection et sur l’injecteur coïncident.

Élimination de l’aiguille
Retirez l’aiguille immédiatement après chaque utilisation de l’injecteur.
11.Insérez délicatement l’aiguille dans le grand capuchon extérieur que vous avez conservé. Ne touchez pas l’aiguille pour éviter toute piqûre.

12.Dévissez l’aiguille en dévissant le grand capuchon extérieur dans le sens contraire des aiguilles d’une montre.
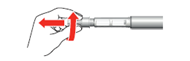
13.Éliminez l’aiguille avec le grand capuchon extérieur dans un récipient étanche que vous recevrez dans votre pharmacie ou auprès de votre service de soins.
14.Fermez l’injecteur avec le capuchon de l’injecteur.
Conservation de l’injecteur
Ne laissez pas l’injecteur avec l’aiguille vissée car cela pourrait provoquer des bulles d’air dans la cartouche. Fermez toujours l’injecteur avec son capuchon.
Élimination de l’injecteur
Le jour de la dernière injection (voir journal d’injection) vous devez jeter l’injecteur. Jetez l’injecteur même s’il reste du médicament dans la cartouche. Jetez l’injecteur en suivant les instructions de votre médecin ou pharmacien(ne).
Fermez l’injecteur avec son capuchon avant de le jeter. Ne jetez pas l’injecteur avec une aiguille fixée dessus.
Que faire si… ?
Bulle d’air dans la cartouche:
vous pouvez utiliser l’injecteur sans problème.
Lors de la préparation de la première injection, aucun liquide ne s’écoule:
Exécutez une nouvelle fois les étapes 5 à 11 comme décrit sous «Préparation de l’injecteur
avant la première injection».
Le bouton d’injection semble bloqué ou vous avez l’impression que l’injection a été insuffisante:
Ne vous réinjectez pas le même jour. Procédez à la prochaine injection le lendemain. Assurez-vous que le chiffre «80» est entièrement visible et centré dans la fenêtre de dose, que la marque blanche est visible dans l’évidement de la fenêtre de dose et que les deux marques imprimées sur le bouton d’injection et sur l’injecteur coïncident.
Source : Swissmedicinfo.ch
Remarques :
– L’équipe de Creapharma.ch a copié à la main le contenu de Swissmedicinfo le 21.12.2022, attention il ne s’agit pas de la date de mise à jour de la notice du médicament, la date de dernière mise à jour de la notice du médicament est mentionnée dans dans un paragraphe en gras ci-dessus.
– Comme information interne à Creapharma.ch, il s’agit de la 1ère publication de cette page depuis le lancement début 2021 de cette rubrique.
– Swissmedicinfo informe via son site Internet les médicaments mis à jour (via rubrique “Textes modifiés”). Creapharma.ch s’engage dans un délai maximum de 30 jours à mettre à jour chaque page médicament provenant de Swissmedicinfo (rubrique Informations destinées aux patients). Cela signifie que pendant quelques jours cette page ne puisse pas être 100% mise à jour. Pour une information toujours mise à jour (actuelle), consultez directement le site Swissmedicinfo.


